RANOLAZIN (RANEXA) BEI CHRONISCH STABILER ANGINA PECTORIS
Im zweiten Anlauf erhält jetzt Ranolazin (RANEXA) die europäische Zulassung zur symptomatischen Behandlung der chronisch stabilen Angina pectoris. Die Indikation ist beschränkt auf die Zusatztherapie, wenn Erstwahlmittel wie Betablocker oder Kalziumantagonisten nicht ausreichen oder nicht toleriert werden. Der bereits in den 1980er Jahren entwickelte und 1986 patentierte antianginöse Wirkstoff ist in den USA für diese Indikation schon seit 2006 zugelassen. Der erste Versuch einer europäischen Zulassung scheiterte im Jahr 2004, weil die Unterlagen grobe Mängel aufwiesen.1
EIGENSCHAFTEN: Der Wirkmechanismus des Piperazinderivates ist nicht vollständig geklärt. Ranolazin hemmt während des Aktionspotenzials selektiv den späten Einwärtsstrom von Natriumionen in kardiale Myozyten, der vor allem in ischämischen Myokardarealen verstärkt ist. Der späte Natrium-Einwärtsstrom zieht über den Natrium-Kalzium-Austauscher eine intrazelluläre Kumulation von Kalziumionen nach sich, die wiederum zur elektrischen Instabilität, erhöhten kardialen Wandspannung, reduzierten Kontraktilität und zellulären Schädigung führt. Diesen Pathomechanismus soll Ranolazin zumindest teilweise unterbrechen. Im Ergebnis wird der Sauerstoffverbrauch vermindert.1,2
Ranolazin wirkt antagonistisch an adrenergen und agonistisch an serotonergen Rezeptoren. Die Bedeutung ist allerdings unklar, zumal das Mittel keinen relevanten Einfluss auf Herzfrequenz, Blutdruck, koronaren Blutfluss und myokardiale Kontraktilität besitzen soll. Metaboliten von Ranolazin stimulieren Opioidrezeptoren, klinisch wird dem aber keine Bedeutung beigemessen. Gleiches gilt für eine Minderung der Oxidation von Fettsäuren.1,2

KLINISCHE WIRKSAMKEIT: Für die Zulassung sind drei randomisierte Doppelblindstudien relevant.4-6 Die MARISA*-Studie4 dient zur Dosisfindung. 191 Patienten nehmen nach Absetzen ihrer antianginösen Therapie im Cross-over je eine Woche lang zweimal täglich 500 mg, 1.000 mg oder 1.500 mg Ranolazin ein oder Plazebo. Im Belastungstest zwölf Stunden nach der letzten Medikation verbessert sich die Belastungsdauer geringfügig, aber signifikant um 24, 34 und 46 Sekunden gegenüber Plazebo; die Zeit bis zum Auftreten pektanginöser Beschwerden nimmt um 27, 46 und 60 Sekunden zu.4
| * | MARISA = Monotherapy Assessment of Ranolazine In Stable Angina |
In die CARISA**-Studie5 werden 823 im Mittel 64 Jahre alte Patienten aufgenommen, die im Belastungstest trotz antianginöser Therapie mit täglich 50 mg Atenolol (TENORMIN, Generika; 43%), 5 mg Amlodipin (NORVASC, Generika; 31%) oder 180 mg Diltiazem (DILZEM, Generika; 26%) typische Anginabeschwerden und EKG-Veränderungen aufweisen. Sie nehmen zusätzlich täglich zweimal 750 mg (maximale zugelassene Dosierung) oder 1.000 mg Ranolazin oder Plazebo ein. 78% der Teilnehmer sind Männer, 64% haben einen Bluthochdruck, 23% einen Diabetes, 29% eine Herzinsuffizienz, 22% eine instabile Angina und 58% einen Herzinfarkt in der Vorgeschichte. Im Belastungstest nach zwölf Wochen nimmt die mittlere Ausdauer im Plazebovergleich unter den beiden Ranolazindosierungen jeweils um 24 Sekunden zu (p < 0,03), die Zeit bis zu anginösen Beschwerden um 30 bzw. 26 Sekunden (p < 0,01 bzw. p < 0,03). Pro Woche verhindert Ranolazin im Mittel einen Anginaanfall.5 Die Ergebnisse sind unabhängig von der antianginösen Basistherapie, die allerdings vor Studienbeginn nicht optimiert wird.
| ** | CARISA = Combination Assessment of Ranolazine In Stable Angina |
In die ERICA***-Studie6 werden 565 im Mittel 62 Jahre alte Patienten mit koronarer Herzkrankheit und mehr als drei Anginaanfällen pro Woche trotz Einnahme von täglich 10 mg Amlodipin aufgenommen. Sie erhalten sechs Wochen lang zusätzlich Ranolazin in der hierzulande nicht zugelassenen Dosierung von zweimal 1.000 mg oder Plazebo. Zuvor eingenommene langwirksame Nitrate (45% der Patienten) dürfen weiter verwendet werden, andere antianginöse Mittel sind verboten. 73% der Patienten sind Männer, 90% haben einen Bluthochdruck, 19% einen Diabetes, 52% eine Herzinsuffizienz, 36% eine instabile Angina und 80% einen Herzinfarkt in der Vorgeschichte. Die mittlere Rate wöchentlicher Anginaanfälle nimmt von 3,3 unter Plazebo auf 2,9 unter Ranolazin ab (p = 0,028), die mittlere Häufigkeit des Nitrogebrauchs zur Anfallskupierung von 2,7 auf 2,0 (p = 0,014). Der Effekt von Ranolazin bei Patienten mit gleichzeitiger Nitrat-Dauertherapie unterscheidet sich nicht von dem in der Gesamtgruppe.6
| *** | ERICA = Efficacy of Ranolazine In Chronic Angina |
Subgruppenanalysen von CARISA und ERICA weisen darauf hin, dass Frauen hinsichtlich Ausdauer und Zeit bis zu anginösen Beschwerden im Belastungstest nicht von Ranolazin profitieren. Die Zahl der Anginaanfälle und der Gebrauch von Nitropräparaten wird jedoch bei Frauen und Männern in gleicher Weise vermindert.7
In keiner der Studien wird für eine optimale antianginöse Basistherapie gesorgt, die als Erstwahlmittel Betablocker umfasst sowie - anstelle von Betablockern oder ergänzend - als Mittel der zweiten Linie langwirksame Nitrate oder Kalzium- antagonisten. Ob Ranolazin bei Patienten mit Beschwerden trotz optimaler antianginöser Therapie einen Zusatznutzen hat, ist somit nicht untersucht. Der Hersteller hat aus der CARISA-Studie eine Post-hoc-Subgruppenanalyse nachgereicht, in der 249 Patienten (30%) ausgewertet werden, bei denen z.B. wegen niedriger Blutdruck- oder Pulswerte die in der Studie vorgeschriebene Einstoff-Basistherapie bereits als "maximal dosiert" angesehen werden kann und die von Ranolazin ebenso profitieren sollen wie die Gesamtgruppe.1 Eine solche nachträgliche Analyse ist wenig aussagekräftig und kann die regelrechte prospektive Prüfung nicht ersetzen.
Die MERLIN-TIMI**** 36-Studie8 untersucht Ranolazin zusätzlich zur Standardtherapie bei Patienten mit akutem Koronarsyndrom ohne ST-Hebung und damit außerhalb der zugelassenen Indikation. 6.560 Patienten erhalten innerhalb von 48 Stunden nach dem Ereignis und dann knapp ein Jahr lang entweder zweimal täglich 1.000 mg Ranolazin oder Plazebo. Der primäre kombinierte Endpunkt aus kardiovaskulären Todesfällen, Infarkten und erneuten Ischämien wird nicht signifikant beeinflusst (21,8% vs. 23,5%; p = 0,11). Die Mortalität ist in beiden Gruppen gleich (Hazard Ratio 0,99). Die signifikante Reduktion erneuter Ischämien unter Ranolazin (13,9% vs. 16,1%; p = 0,03) ist als antianginöser Effekt erklärbar.1,2
| **** | MERLIN-TIMI = Metabolic Efficiency with Ranolazine for Less Ischemia in Non-ST-Elevation Acute Coronary Syndromes |
VERTRÄGLICHKEIT: Ranolazin hat eine geringe therapeutische Breite. Mit zunehmender Dosis nehmen Häufigkeit und Schwere unerwünschter Wirkungen zu. Unter den zugelassenen Dosierungen kommen am häufigsten Obstipation, Übelkeit, Bauchschmerz, Erbrechen, Schwäche und Schwindel vor. Sie sind bis zu 10% häufiger als unter Plazebo und Hauptgründe für einen Abbruch der Therapie wegen Nebenwirkungen (1% bis 4%).1,2,8 Im oberen Dosisbereich nehmen auch Sehstörungen, Somnolenz, Lethargie und andere zentralnervöse Nebenwirkungen zu.1 Unter Ranolazin verlängert sich die QTc-Zeit im Mittel um 5 ms bis 15 ms.4,5 Sporadisch und dosisabhängig ist die QTc-Verlängerung aber deutlicher: Unter der nicht zugelassenen Dosis von zweimal 1.000 mg beträgt sie bei etwa 4% der Patienten mehr als 60 ms.1 Eine Häufung ventrikulärer Rhythmusstörungen ist bisher nicht beschrieben. Die ROLE*****-Nachbeobachtung9 von 746 Patienten aus zwei Zulassungsstudien über knapp drei Jahre erfasst vierzehn plötzliche Todesfälle und vier tödliche ventrikuläre Arrhythmien unter Ranolazin. In den Zulassungsstudien fallen acht Synkopen unter Verum auf (Plazebo: keine).4,5 Bei Patienten mit akutem Koronarsyndrom sind Synkopen unter Ranolazin signifikant häufiger als unter Plazebo (3,3% vs. 2,3%; p = 0,01). Sie werden überwiegend als vagovasal gedeutet.1,8
| ***** | ROLE = Ranolazine Open Label Experience |
WECHSELWIRKUNGEN: Wechselwirkungen sind häufig. Starke Hemmstoffe von CYP3A4 wie das Azolantimykotikum Itraconazol (SEMPERA, Generika) oder das Makrolid Clarithromycin (KLACID; Generika) können die Ranolazinspiegel bis zum Vierfachen erhöhen und sind kontraindiziert. Bei mäßigen Hemmstoffen von CYP3A4 wie z.B. Erythromycin (ERYHEXAL u.a.) oder von p-Glykoprotein wie z.B. Verapamil (ISOPTIN, Generika) ist besondere Vorsicht geboten. Gleichzeitige Einnahme von CYP3A4-Induktoren wie Carbamazepin (TEGRETAL, Generika) vermindert die Plasmakonzentration von Ranolazin deutlich, es sollte dann nicht verordnet werden. Vorsicht: Unter Behandlung mit Ranolazin können die Spiegel von Herzglykosiden, Statinen, trizyklischen Antidepressiva und Neuroleptika ansteigen. Kombination mit Mitteln, die ebenfalls die QTc-Zeit verlängern (z.B. trizyklische Antidepressiva), sollte vermieden werden.1,3 Komedikation mit Antiarrhythmika der Klasse Ia und III ist kontraindiziert.3
Angesichts der langen Liste der potenziell lebensbedrohlichen Wechselwirkungen und Gegenanzeigen schreibt die europäische Zulassungsbehörde EMEA eine so genannte Patienten-Informations-Karte (PIK) vor, die die Patienten bei allen Arztbesuchen mit sich führen sollen und die die Patienten selbst und das medizinische Personal über kontraindizierte Arzneimittel und risikobehaftete Begleitumstände bei Gebrauch von Ranolazin informiert.1
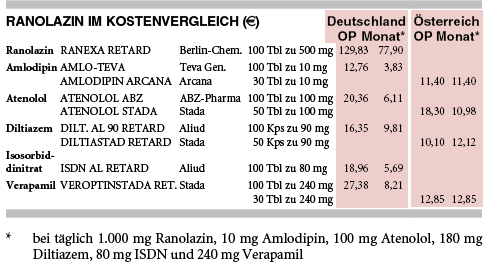
KOSTEN: Bei Monatskosten von 78 € verteuert Ranolazin (RANEXA, 2 x 500 mg/Tag) die Therapie gegenüber der mit Generika wie Amlodipin (AMLO-TEVA, 4 €, 10 mg/Tag), Atenolol (ATENOLOL ABZ, 6 €, 100 mg/Tag), Diltiazem (DILTIAZEM AL 90 RET., 10 €, 2 x 90 mg/Tag), Isosorbiddinitrat (ISDN AL RET., 6 €, 80 mg/Tag) oder Verapamil (VEROPTINSTADA RET., 8 €, 240 mg/Tag) bis zum 20fachen.
Mit Ranolazin (RANEXA) ist ein neues Mittel zur symptomatischen Therapie der chronisch stabilen Angina pectoris zugelassen, wenn Standardmittel nicht ausreichen.
Ranolazin hemmt den langsamen Natriumeinstrom während des Aktionspotenzials.
Ranolazin ähnelt in seinen Wirkungen einem Kalziumantagonisten, hat aber keinen relevanten Einfluss auf Blutdruck und Herzfrequenz.
Zusätzlich zu Betablockern oder Kalziumantagonisten eingenommenen verbessert es die Belastungstoleranz nur geringfügig: Pro Woche werden im Mittel 0,4 bis maximal ein Angina-pectoris-Anfall verhindert.
Ranolazin ist nicht bei Patienten geprüft, die trotz optimaler antianginöser Therapie weiterhin Beschwerden haben. Sein Stellenwert in der zugelassenen Indikation ist deshalb nicht beurteilbar.
Die Prognose der koronaren Herzkrankheit wird durch das Mittel nicht verbessert.
Ranolazin wird vorwiegend über CYP3A4 metabolisiert. Vielfältige relevante Wechselwirkungen sind bekannt.
Die QT-Zeit wird im Mittel nur gering, dosisabhängig in bis zu 4% aber deutlich verlängert. Plötzliche Todesfälle unter Ranolazin sind beschrieben.
Obstipation, Übelkeit, Schwäche und Schwindel sind die häufigsten Störwirkungen. Bei bis zu einem von hundert Patienten kommt es zu Synkopen.
Wir erachten die Nutzen-Schaden-Bilanz von Ranolazin beim derzeitigen Kenntnisstand als negativ. Eine Indikation sehen wir nicht.
| (R = randomisierte Studie) | ||
| 1 | EMEA: Europ. Beurteilungsbericht (EPAR) RANEXA, Stand 11. Febr. 2009 http://www.emea.europa.eu/humandocs/Humans/EPAR/ranexa/ranexa.htm | |
| 2 | NASH, D.T., NASH, S.D.: Lancet 2008; 372: 1335-41 | |
| 3 | Berlin-Chemie: Fachinformation RANEXA, Stand Nov. 2008 | |
| R | 4 | CHAITMAN, B.R. et al.: J. Am. Coll. Cardiol. 2004; 43: 1375-82 |
| R | 5 | CHAITMAN, B.R. et al.: JAMA 2004; 291: 309-16 |
| R | 6 | STONE, P.H. et al.: J. Am. Coll. Cardiol. 2006; 48: 566-75 |
| 7 | WENGER, N.K. et al.: Am. J. Cardiol. 2007; 99: 11-8 | |
| R | 8 | MORROW, D.A. et al.: JAMA 2007; 297: 1775-83 |
| 9 | KOREN, M.J. et al.: J. Am. Coll. Cardiol. 2007; 49: 1027-34 |
© 2009 arznei-telegramm, publiziert am 6. März 2009
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
