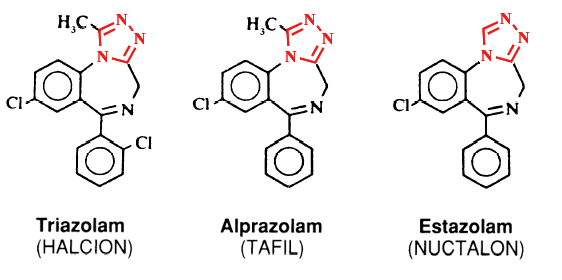
Das ultrakurz wirkende Benzodiazepin Triazolam (HALCION) gehört Alprazolam (TAFIL) und Estazolam [NUCTALON, Frankreich]) zur Gruppe der
Triazolo-Derivate (vgl. Abbildung). Diesen werden von anderen Benzodiazepinen abweichende Eigenschaften zugeschrieben. Triazolam und Alprazolam führen
die Liste von Arzneistoffen an, die mit der Auslösung aggressiven Verhaltens in Verbindung gebracht werden.1
Patienten mit Entzugserscheinungen nach Absetzen dieser Benzodiazepine sprechen nicht immer auf Diazepam (VALIUM u.a.) oder Phenobarbital (LUMINAL u.a.)
an.2 Psychische Störwirkungen wie Depression und Paranoia sind dokumentiert.3
In einem "Dear Doctor Letter" informiert das Britische Komitee für Arzneimittelsicherheit, daß ab 2. Oktober 1991 wegen
Sicherheitsmängeln das Benzodiazepin Triazolam (HALCION) in allen Anwendungsformen vom Markt genommen werde.
Im Vergleich zu anderen Benzodiazepinen treten unter Triazolam wesentlich häufiger reversible psychiatrische Störungen auf, insbesondere
Gedächtnislücken und Depressionen. Dies habe die englische Zulassungsbehörde erst kürzlich erfahren. Die bisherige Annahme, solche
Reaktionen seien nur für hohe Dosen von Triazolam (1 mg oder mehr) bekannt, erscheint überholt. Gleichartige Probleme kommen auch im niedrigen
Dosierungsbereich von Triazolam zwischen 0,125 bis 0,25 mg vor. Nach dem gegenwärtigen Stand des Wissens liege die therapeutische Breite (Abstand
zwischen wirksamer und schädlicher Dosis) für Triazolam in einem inakzeptablen Bereich. Die Risiken seiner Anwendung überwiegen den
Nutzen.
Die behördlich angeordnete Marktrücknahme in Großbritannien, so der "Dear Doctor Letter", könne in Einzelfällen
Schwierigkeiten mit sich bringen. Gegebenenfalls könne alternativ ein anderes Benzodiazepin verschrieben werden, wenn ein Hypnotikum unbedingt
erforderlich sei. Generell wird aber daran erinnert, daß die ununterbrochene Einnahme 28 Tage nicht übersteigen darf, wenn ein Benzodiazepin eingesetzt
wird.4
Am 2. Oktober 1991 setzte das Bundesgesundheitsamt die Firma Upjohn in Heppenheim von der Absicht in Kenntnis, das Ruhen der Zulassung für Arzneimittel
mit dem Wirkstoff zunächst befristet bis zum 29. Februar 1992 anzuordnen.
Es bestehe der begründete Verdacht, daß zentralnervöse Nebenwirkungen wie Erregung, Angst, Aggressivität, Depression und Amnesien unter
Triazolam auch in niedriger Dosierung häufiger und gravierender sind, als bisher angenommen wurde. Da für HALCION "in den beanspruchten
Anwendungsgebieten therapeutische Alternativen vorhanden sind, die derartige Risiken nicht in dem genannten Maße aufweisen", sieht die deutsche
Gesundheitsbehörde die Anwendung von Triazolam "als medizinisch nicht mehr vertretbar" an.5
Unterlagen, die bei der US-amerikanischen Food and Drug Administration in Washington von HALCION-Kritikern eingesehen werden konnten, bringen das US-
Pharmaunternehmen Upjohn ins Zwielicht. Upjohn bediente anscheinend weltweit die Gesundheitsbehörden mit geschönten Nebenwirkungsangaben.
Für das Bundesgesundheitsamt stellt sich jetzt erst heraus, "daß zentralnervöse Nebenwirkungen in einer Studie ..., die einer Zulassung mit der
Dosisstärke von 1 mg im Jahr 1979 zugrunde gelegen hat, weitaus häufiger waren, z.T. doppelt so hoch, wie es in den uns bislang vorliegenden
Unterlagen dokumentiert war".
Das BGA wertet das vorgesehene befristete Ruhen der Zulassung gegenüber dem Widerruf der Zulassung als minderschwere Maßnahme. Sie sei
erforderlich, "um bis zur hinreichenden Klärung der aufgetretenen erheblichen Risiken einen wirksamen Schutz der Patienten
sicherzustellen".
Uns war das HALCION-Problem vor der Einführung des Wirkstoffs in Deutschland bekannt. Schon im a-t 8 (1979), 65 warnten wir erstmals vor dem
"Horror-Hypnotikum" Triazolam. Wegen des VAN-DER-KROEF-Syndroms, Rebound-Angst, Rebound-Schlaflosigkeit, Amnesie (insbesondere in
Kombination mit Alkohol), psychischen Störungen und Suizidalität forderten wir Anwendungsbeschränkungen (a-t 11 [1987], 100). Es wurde jedoch
nur die 0,5-mg-Zubereitung wegen erhöhter Nebenwirkungshäufigkeit verboten (a-t 1 [1988], 6). Die Komplikationsdichte von HALCION-Niedrigdosen im
Vergleich zu anderen Benzodiazepinen beschrieben wir an anderer Stelle.6,7
Auch nachdem HALCION in die Schlagzeilen geriet, versuchte der pharmazeutische Unternehmer Warnungen mit Appellen an die Ärzteschaft zu unterlaufen:
"Ihre älteren Patienten haben gute Gründe, Ihnen zu vertrauen – Sie haben gute Gründe, ihnen HALCION zu verschreiben!
"
Upjohn-Werbestrategen nannten "individuelle Gründe ..., einleuchtende Gründe ..., erfrischende Gründe" und schließlich
"populäre Gründe: Denn HALCION ist weltweit die Nr. 1".8
Der Appell kam an, denn HALCION wird in der Bundesrepublik ungebrochen weiter verordnet. Das Mittel steht in der Rangskala der 500 meistverordneten
Arzneimittel der Bundesrepublik. HALCION wird hierzulande in Mengen verkauft, die Upjohn einen Jahresumsatz von über 10 Millionen DM einbringen.
Wenn Gesundheitsbehörden nach langem Zögern wirksame Abwehrmaßnahmen ergreifen oder ergreifen wollen, machen sie die Rechnung ohne
den Wirt. In der Presseinformation der Upjohn GmbH vom 9. Oktober lesen wir: "Klinische Prüfung und umfangreiche Erfahrungen mit den Patienten
haben den Nachweis erbracht, daß HALCION ein sicheres Arzneimittel ist, wenn es vorschriftsmäßig angewandt wird".
Welcher Patient kann der ärztlichen Verordnung von HALCION Vertrauen entgegenbringen, wenn er den Verbotstatus von HALCION in Großbritannien
und Finnland aus der Zeitung erfährt und das Verbot auf nachvollziehbaren und einleuchtenden Gründen beruht?
Daß sich Upjohn in einem zivilgerichtlich anhängigen Prozeß um die Abfindung von HALCION-Folgen mit einem Schweigegeld in Millionenhöhe
der Peinlichkeit entzog, daß Arzneimittelsachverständige vor Gericht Triazolam-Beurteilungen abgeben, macht nachdenklich, weil es nicht zum Prozedere
vertrauensbildender Maßnahmen gehört.
|
WAS SPRICHT GEGEN TRIAZOLAM (HALCION)?
nach AYD, F. J.: Intern. Drug Therap. Newsletter 26 (1991), 25
- Erinnerungsstörungen am Tag nach der Einnahme traten in einer Vergleichsstudie mit Temazepam (PLANUM u.a.) und Plazebo unter Triazolam alarmierend
häufig (40%) auf, nicht aber unter Temazepam.
- Für die niedrigere Dosis von 0,25 mg Triazolam zeigen kontrollierte Studien eine Abnahme der Wirksamkeit, aber immer noch häufige und
schwerwiegende unerwünschte Effekte. Folglich mindert die Dosisreduktion den Nutzen von Triazolam ausgeprägter als die Risiken.
- In kontrollierten Studien sind unter Triazolam-Erregungszustände dokumentiert (Schlaflosigkeit am frühen Morgen, Angst unter Tage, Panikattacken
und manische Episoden, organisches Hirnsyndrom in Form von Erinnerungsstörungen und anderen kognitiven Fehlleistungen) sowie Absetzphänomene
(Rebound-Schlaflosigkeit und Rebound-Angst).
- Die für Triazolam-berichtete Nebenwirkungskasuistiken umfassen kognitive Fehlleistungen (Erinnerungsstörungen, Amnesie, Verwirrtheit,
Desorientierung, paranoide Reaktionen und andere wahnhafte Verkennungen sowie Halluzinationen), Erregungszustände (Schlaflosigkeit in den frühen
Morgenstunden, Angst unter Tage, Spannungszustände, Enthemmung, Panikattacken und manische Episoden) sowie Absetzphänomene (Rebound-
Schlaflosigkeit und Krämpfe).
- Im Vergleich zu Temazepam und Flurazepam sind im FDA-Register ZNS- und Verhaltensstörungen für 0,5 mg Triazolam um das 5- bis 10fache
häufiger und für die 0,25-mg-Dosis um das 3- bis 13fache häufiger erfaßt worden als für entsprechende Dosen anderer
Benzodiazepine.
- Filmrißepisoden, Verhaltensauffälligkeiten, Halluzinationen, Reizbarkeit (in Form von Aggressivität und Wutausbrüchen) sowie Tod werden im
FDA-Register für Triazolam auffällig häufig erfaßt. Beim Vergleich mit 100 anderen Wirkstoffen steht Triazolam hier an erster Stelle.
- Experimentelle Befunde korrelieren mit dem besonderen Nebenwirkungsprofil von Triazolam. Dieses Benzodiazepin-Derivat fällt durch seine ultrakurze
Halbwertszeit sowie durch seine extrem hohe Affinität zum Rezeptor auf.
- Triazolam ist wegen Berichten über Depression, Psychosen und schwerwiegende Verhaltensstörungen gerichtsbekannt.
FAZIT: Im Vergleich mit anderen Benzodiazepinen scheinen Derivate mit Triazol-Struktur vom Typ des Triazolam (HALCION) Wirkungen zu besitzen, die
deutlich vom üblichen Benzodiazepinwirktyp abweichen. Wegen des ungünstigen Nutzen-Risiko-Verhältnisses sollte Triazolam (HALCION) verboten
und andere Triazolo-Verbindungen wie Alprazolam (TAFIL) der verschärften Beobachtung unterstellt werden.
|
Die HALCION-Risikodaten dürfen nach Auffassung der Upjohn Company in den USA als "Betriebsgeheimnisse" nicht in die Öffentlichkeit
gelangen – auch nicht durch Sachverständige.9 Daß sich hier der pharmazeutische Anbieter bemühte, die Aufdeckung der
Datenunstimmigkeit bei Zulassungsbehörden zu verhindern, muß die Öffentlichkeit ebenso beunruhigen wie die Wirkung eines Schlaf- und
Beruhigungsmittels aus der Benzodiazepinreihe, das paradoxerweise erregt statt beruhigt. Um den Schlaf gebracht sieht sich auch der Erstbeschreiber der
Triazolam-Unverträglichkeiten, der holländische Psychiater VAN DER KROEF. Die überfallartig einsetzende Triazolam-Wirkung raube dem
Verwender die Chance, seinen geänderten Bewußtseinszustand wahrzunehmen. Kein länger wirkendes Benzodiazepin könne innerhalb kurzer
Zeit so starke Veränderungen auslösen. "Die sozialen Konsequenzen und sogar das kriminelle Potential von Triazolam sind furchterregend. Die
HALCION-Gebrauchsinformation läßt hierüber den Patienten im Unklaren."10

|


