14 MONATE TICOVAC - EINE CHRONIK
Februar 2000
Die Firma Baxter ersetzt ihren seit 1982 erhältlichen FSME-Impfstoff FSME-IMMUN durch TICOVAC. Bei der neuen Vakzine wird auf das
Quecksilberkonservans und auf Albumin als Stabilisator verzichtet. Baxter hätte den Impfstoff - wie bei solchen Produktveränderungen üblich -
beispielsweise auch FSME-IMMUN SINE nennen können. Wegen der EU-Zulassung entscheidet sich die Firma jedoch europaweit für das Warenzeichen
TICOVAC. Baxter betont die gute Verträglichkeit: "Publikationen zur FSME-Impfung und dem Vorgängerprodukt FSME-IMMUN Immuno belegen die
sehr gute Verträglichkeit der FSME-Impfstoffe" (Baxter: "Kompendium FSME, Druckzeichen PR63F 01/00, Seite 30). Schon bei der Erprobung
waren jedoch überdurchschnittlich häufig Fieberreaktionen aufgefallen, ohne dass hieraus Konsequenzen gezogen werden. Lediglich in der
Produktinformation findet sich der Hinweis, dass "bei Kindern gehäuft Fieber bis über 38° C auftreten" kann, insbesondere nach der 1.
Teilimpfung (TICOVAC Fachinformation, Stand Jan. 2000).
TICOVAC wird für Kleinkinder, Kinder und Erwachsene beworben. In einem Prospekt weist Baxter auf angeblich "schwere Verläufe" von
FSME-Infektionen bei Kindern mit der Folge von "Defektzuständen" hin: "Bei Untersuchung von 133 Kindern, die in Slowenien auf Grund einer
FSME-Infektion auf eine Intensivstation aufgenommen wurden, war bei ca. 5% der Kinder eine intensivmedizinische Behandlung nötig" (Baxter:
"Kompendium FSME", Seite 24).
März 2000
Wegen einer Flut von Spontanberichten zu Fieberreaktionen insbesondere nach der ersten Teilimpfung und der Gefahr von Fieberkrämpfen empfiehlt der
Hersteller in einem Rote-Hand-Brief, Kindern bis zum 15. Lebensjahr nur noch die halbe Dosis (0,25 ml) zu spritzen (Pharm. Ztg. 2000; 145: 991). Die Häufung
der Unverträglichkeitsreaktionen führt man darauf zurück, dass die Hilfsstoffe des alten FSME-IMMUN, die die Immunreaktion gedämpft haben
könnten, beim "reineren" TICOVAC fehlen (BEICHE, Baxter, persönl. Mitteilung vom 31. März 2000). Dies erinnert an die Argumentation
der Chiron Behring GmbH, die 1998 den Kinderimpfstoff ENCEPUR K auf Grund erhöhter Melderaten von allergischen/pseudoallergischen Reaktionen vom
Markt zog. Als Auslöser galt damals ein Zusammenwirken der Hilfsstoffe Aluminiumhydroxid und Polygelin (a-t 1998;
Nr. 5: 51). Baxter betont daher im Einführungsprospekt: "TICOVAC ist der einzige FSME-Impfstoff in Deutschland, der kein Polygelin
enthält" (Baxter: "Kompendium FSME, Seite 30).
April 2000
Auf unsere Frage, wie die Wirksamkeit der halbierten Dosis für Kinder belegt ist, verweist Baxter auf interne Untersuchungen mit Daten zu
Serumkonversionsraten (Baxter: Schreiben vom 12. Apr. 2000). In einer Zusammenfassung der Studien teilen Firmenautoren mit: "Es steht außer Zweifel,
dass Kinder ebenso wie Erwachsene in den Endemiegebieten Europas hinsichtlich einer Infektion mit dem FSME-Virus gefährdet sind" (Manuskript von
EDER, G. et al.: "Dosisanpassung der FSME-Impfung für Kinder"). Für Ende des Jahres 2000 kündigt Baxter eine spezielle Zubereitung
für Kinder an: TICOVAC JUNIOR.
Mai 2000
Bereits drei Monate nach der Markteinführung entfallen in unserem NETZWERK DER GEGENSEITIGEN INFORMATION 15% aller 335 Berichte zu FSME-
Impfstoffen auf die Neueinführung TICOVAC. Auch die inzwischen empfohlene reduzierte Dosis wird von Kindern nicht vertragen (a-t 2000; 31: 55).
Der Hersteller kündigt "sobald als möglich zusätzliche Dosisoptimierungsstudien in Erwachsenen und Kindern" an (Baxter: Schreiben vom
29. Mai 2000). "Offensichtlich soll jetzt nachgeholt werden, was bei Erprobung und Zulassung des neuen Impfstoffes versäumt worden ist" (blitz-a-t vom 30. Mai 2000).
Das Paul-EHRLICH-Institut (PEI) teilt uns mit, allein keine Maßnahmen zur Risikoabwehr durchführen zu können, da TICOVAC im
europäischen Verfahren der gegenseitigen Anerkennung zugelassen ist (PEI: Schreiben vom 31. Mai 2000).
Juni 2000
Drei Wochen später besinnt sich das PEI auf die im EU-Recht vorgesehene Möglichkeit von Notfallmaßnahmen ("Urgent Safety
Restriction") und schränkt die Anwendung von TICOVAC ein:
 Keine Impfung von Kindern unter 3 Jahren, Keine Impfung von Kindern unter 3 Jahren,
 Halbierung der Dosis auf 0,25 ml für ältere Kinder und Jugendliche bis 15
Jahren sowie Halbierung der Dosis auf 0,25 ml für ältere Kinder und Jugendliche bis 15
Jahren sowie
 Impfung nur für Personen, die sich in einem nach offiziellen Empfehlungen
ausgewiesenen FSME-Hochrisikogebiet aufhalten. Impfung nur für Personen, die sich in einem nach offiziellen Empfehlungen
ausgewiesenen FSME-Hochrisikogebiet aufhalten.
Auch bei Erwachsenen werden häufiger Fieber-Reaktionen beobachtet, "als man es bisher kannte" (PEI: Information für Ärzte und
Apotheker vom 21. Juni 2000). Erst durch die breite Anwendung von TICOVAC sei deutlich geworden, in welch starkem Maße Fieberreaktionen
auftreten.
Das PEI hält jetzt "auf Grund einer erneuten Nutzen-Risiko-Abschätzung" die Impfung von Säuglingen und Kleinkindern wegen der
Gefährdung durch hohes Fieber und damit verbundene Fieberkrämpfe für riskant. "Bei Kindern unter vier Jahren tritt die Frühsommer-
Meningoenzephalitis nur sehr selten auf und verläuft dann auch verhältnismäßig mild. Vor allem aber hinterlässt sie keine bleibenden
Schäden." Für ältere Kinder bleibt das PEI bei der Positivbewertung der Impfmaßnahme:
"Trotz einer ungewöhnlich hohen Zahl von Nebenwirkungsmeldungen ... sind wir auf den Impfstoff TICOVAC angewiesen, um Kinder über drei Jahre
vor der Frühsommer-Meningoenzephalitis (FSME) zu schützen," kommentiert Instituts-Leiter LÖWER. Er stützt sich dabei nicht auf
kontrollierte Studien mit klinischen Endpunkten, in denen Komplikationen bei Geimpften und Erkrankungen Nichtgeimpfter verglichen werden, sondern lediglich auf
Untersuchungen zum Surrogatkriterium Titeranstieg.
Unser Fazit: "Um ein extrem seltenes Ereignis mit einer infektionsbedingten bleibenden Schädigung beim Kind zu verhindern, akzeptiert das PEI
regelmäßig auftretende, zum Teil Tage anhaltende gravierende Impfreaktionen. Da stimmt die Nutzen-Schaden-Bilanz nicht... Logische Konsequenz ist,
den unkontrollierten Feldversuch abzubrechen und das unzureichend geprüfte TICOVAC schleunigst vom Markt zu nehmen" (a-t 2000; 31: 64).
Juli 2000
Unsere Anfrage, welche und wie viele Meldungen dem PEI vorliegen, wird ausweichend und nur pauschal ("in der Größenordnung von mehreren
Hundert", "in einigen Fällen auch Fieberkrämpfe") beantwortet (PEI: Schreiben vom 4. Juli 2000). Erst nach Insistieren erhalten wir
nähere Auskunft:
Am 27. Juli 2000, ein halbes Jahr nach Markteinführung, sind bereits 1.119 Verdachtsfälle erfasst. Als unerwünschte Folgen dominieren Fieber (n =
923), Kopfschmerzen (428), Gliederschmerzen (186), Schüttelfrost (159), grippale Beschwerden (75), Nackenschmerzen und/oder Nackensteife (44) und
Meningismus (40). Mehr als die Hälfte der Berichte betreffen unter 16-Jährige. Jedes zweite Kind hat bereits die empfohlene halbierte Dosis von 0,25 ml
erhalten (PEI: Schreiben vom 28. Juli 2000). Diese Häufung beeinträchtigender Störwirkungen erachten wir als "nicht akzeptabel" und
mahnen erneut die Marktrücknahme von TICOVAC an (a-t 2000; 31: 71).
Nach vorübergehenden Engpässen ist das Konkurrenzprodukt ENCEPUR wieder lieferbar (Chiron Behring: Schreiben vom 27. Juli 2000). Die Zeit
höchster Zeckenaktivitäten (in Europa April bis Juli) ist jetzt allerdings weitgehend vorbei. Die Welle impfbedingter Schädigungen ebbt
allmählich ab.
September 2000
Allen behördlichen Maßnahmen und Bedenken zum Trotz geht die Propaganda für die Vakzine weiter: "Gerade für Kinder ist die FSME-
Impfung besonders sinnvoll", titelt die Ärzte Zeitung am 27. Sept. 2000. Weil die passive Immunisierung gegen FSME bei Kindern nicht zugelassen ist,
"ist gerade für Kinder, die in Endemiegebieten leben, die aktive Immunisierung besonders sinnvoll", verkündet ein "Experte".
Weiterhin wird als schlechte Medizin gebrandmarkt, wenn erwogen wird, Kinder nicht zu impfen. "Auch wenn die Beratung zur FSME-Impfung derzeit
umständlich ist und sehr gewissenhaft durchgeführt werden muss, sollte man daraus nicht die Konsequenz ziehen, die Impfung bei Kindern einfach zu
unterlassen" (STÜCK, B. in STÜCK, B. [Hrsg.]: "200 Impffragen aus der pädiatrischen Praxis", Marseille Verlag München, 2000,
Seite 190-1).
Dezember 2000
Der Leiter des PEI kündigt eine Publikation des Nebenwirkungsprofils von TICOVAC für Beginn des Jahres 2001 an (PEI: Schreiben vom 11. Dez.
2000).
Februar 2001
Das PEI kann noch keinen Termin für das Erscheinen der angekündigten Dokumentation des Risikoprofils von TICOVAC nennen (PEI: Schreiben vom
24. Febr. 2001).
Baxter teilt uns auf Anfrage mit, noch in diesem Jahr einen veränderten FSME-Impfstoff anbieten zu wollen (Baxter: Schreiben vom 20. Febr. 2001). Angesichts
des Desasters bei der Umstellung von FSME IMMUN auf TICOVAC stimmt das PEI einer erneuten Produktveränderung jedoch nicht zu und fordert weitere
Studien.
März 2001
Am 1. März stellen Experten auf einer vom PEI einberufenen Anhörung fest, dass sich nach Erfahrungen in Deutschland die Impfung von Kindern mit
TICOVAC nicht vertreten lässt. Mit Wirkung vom 16. März 2001 verzichtet Baxter daraufhin "eigenverantwortlich" auf die Zulassung von
TICOVAC. Die Firma begründet dies, ohne auf die Dimension der eingegangenen Nebenwirkungsberichte einzugehen, mit häufigen Fieberreaktionen, zum
Teil mit raschem Temperaturanstieg bis über 40° Celsius und "gelegentlichen Fieberkrämpfen" sowie mit gehäuften
Allgemeinreaktionen mit Fieber und/oder grippeähnlichen Symptomen bei Erwachsenen (Baxter: Rote-Hand-Brief vom 26. März 2001) - also mit
ähnlichem Wortlaut, mit dem das PEI im Juni 2000, die Indikationseinschränkungen für TICOVAC begründet hat. Zur Impfung von Kindern ab
vollendetem 12. Lebensjahr und Erwachsenen gegen FSME steht seitdem nur noch ENCEPUR zur Verfügung. Für Kinder unter 12 Jahren gibt es keinen
FSME-Impfstoff mehr.
Nun ist es auch PEI und Baxter klar, dass Kinder seltener als Erwachsene an FSME erkranken und bleibende neurologische Schäden im Kindesalter
"eine Rarität" sind. Diese Einschätzung bezieht das PEI jetzt nicht mehr nur auf Kinder unter vier Jahren, sondern auf Kinder und Jugendliche.
"Eine publizierte Kasuistik eines 12-jährigen Jungen mit bleibendem neurologischen Schaden nach einer FSME-Infektion ist der einzige bekannte Fall in
der deutschsprachigen Literatur, bei dem eine FSME-Infektion ohne zusätzliche ärztliche Intervention zu einer neurologischen Dauerschädigung
führte."
Auch eine systematische Abfrage bei Kinderkliniken lässt keine Gefährdung erkennen. Aus 478 angeschriebenen klinisch-pädiatrischen Abteilungen
werden insgesamt 17 FSME-Erkrankungen bei Kindern bis 16 Jahren mitgeteilt (Diagnosen: 14-mal Meningitis, 2-mal Meningoenzephalitis, 1-mal Meningitis und
Cerebellitis). Keines der Kinder ist aktiv oder passiv gegen FSME immunisiert. Bei allen nimmt die Erkrankung "einen blanden Verlauf" mit
vollständiger Wiederherstellung. "Durch die Erhebung des Paul-EHRLICH-Instituts konnte somit kein Fall einer schwer verlaufenden FSME-Erkrankung
bei Kindern bis 16 Jahre im Zeitraum 1997/98 in Deutschland eruiert werden" (PEI: Information für Ärzte und Apotheker vom 28. März 2001).
Angesichts dieser Erkenntnisse erscheint uns TICOVAC ersatzlos entbehrlich.
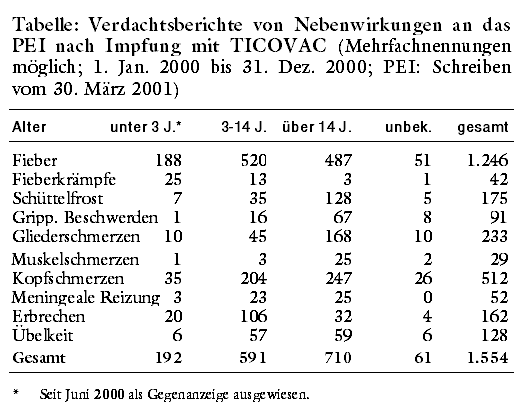
Ende März gibt uns das PEI eine aktuelle statistische Aufstellung der in Verbindung mit TICOVAC erfassten Störwirkungen (s. Tabelle). Insgesamt
1.554 Verdachtsberichte sind erfasst, vor allem Fieber, Kopfschmerzen, Gliederschmerzen, Schüttelfrost und Erbrechen (PEI: Schreiben vom 30. März
2001). Dabei handelt es sich jedoch nur um den kleineren Teil der Nebenwirkungsberichte. Pharamhersteller müssen nur schwerwiegende Verdachtsfälle
innerhalb von 15 Tagen an die zuständige Bundesoberbehörde weitermelden. Bei Baxter sind deutlich mehr nicht-schwerwiegende Verdachtsmeldungen
registriert. Fieberreaktionen hat die Firma 2.947-mal erfasst (1.689 bei Kindern und Jugendlichen, 1.258 bei Erwachsenen). Das ist das 2,4fache der beim PEI
vorhandenen Berichte.
April 2001
Die angekündigte Veröffentlichung einer Dokumentation ist das PEI nach wie vor schuldig geblieben. Mehr als ein Jahr nach Beginn der auffälligen
Häufung von Nebenwirkungsmeldungen, erhalten die Fachkreise nur pauschale Informationen über den Kenntnisstand. Mit der im vergangenen Jahr
selbst formulierten Informationsverpflichtung gegenüber "Verbrauchern und Behandlern" (PEI: Schreiben vom 11. Dez. 2000) tut sich das PEI
schwer.
|

