Darmverschluss durch Medizinprodukt CM3: Eine 56-jährige Frau mit einer 20 Jahre zurückliegenden Darmoperation entwickelt eine
Woche nach Einnahme von drei Kapseln CM3 einen mechanischen Ileus. Der Dünndarm perforiert, das Bauchfell entzündet sich. Teile des Dünn-
und Dickdarms müssen entfernt werden (NETZWERK-Bericht 11.402). Das Produkt aus hochvernetzter Zellulose aus den Rohstoffen Flachs, Baumwolle und
Holzfaser (A + G lifescience: Schreiben vom 2. August 2001) quillt im Magensaft auf und soll durch Füllung des Magens ein Sättigungsgefühl
hervorrufen. Trotz der Bedenken, die unverdaulichen Schwämmchen könnten während der Passage im Verdauungstrakt gefährliche
Verschlüsse verursachen (a-t 1999; Nr. 4: 45 und a-t 1999; Nr. 6:
63), wurde CM3 die angeblich "erfolgreichste OTC* Neueinführung 1999" (A + G lifescience: Pharm. Ztg. 2000; 145: 299). Dem Bundesinstitut
für Arzneimittel und Medizinprodukte (BfArM) liegen insgesamt acht Berichte über Darmverschlüsse in Verbindung mit CM3 vor. Drei Betroffene haben
die in der Packungsbeilage aufgeführten Gegenanzeigen - Darmerkrankungen und zurückliegende Operationen im Bauchraum - nicht beachtet. Auch bei
vier von zwölf weiteren Verdachtsberichten über Verstopfung, Magenausgangsstenose u.a. sollen Kontraindikationen bestanden haben (BfArM:
Schreiben vom 5. Sept. 2001). Lebensbedrohlicher Darmverschluss ist ein unvertretbares Risiko für ein Medizinprodukt, das (ohne hinreichende klinische
Nutzenbelege) zur Selbstmedikation bei Übergewicht angeboten wird. Die Relevanz der im Beipackzettel angegebenen umfangreichen Gegenanzeigen, die
zum Teil nur mit Fachtermini bezeichnet sind, ist für Laien unüberschaubar. CM3 ist u.E. als bedenklich einzustufen. Wir fordern ein sofortiges Verbot, -
Red.
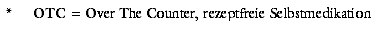
| © 2001 arznei-telegramm |
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
