NUTZEN UND SCHADEN DES MAMMOGRAPHIESCREENINGS
Das Mammographiescreening auf Brustkrebs gilt weithin als gut untersuchte wirksame Früherkennungsmaßnahme, zu der elf randomisierte kontrollierte Studien mit mehr als 650.000 Frauen und Nachbeobachtungszeiten von durchschnittlich zehn Jahren vorliegen.1 Auf Basis der Ergebnisse aus frühen Studien, die bereits seit den 1960er und 1970er Jahren aufgelegt wurden, sind seit 1987 in zahlreichen Ländern regionale oder landesweite Screeningprogramme gestartet worden.2 In Deutschland ist nach einem Beschluss des Deutschen Bundestages von 2002 ab 2005 ein Reihenuntersuchungsprogramm entstanden. 50- bis 69-jährige Frauen werden alle zwei Jahre zu einer Untersuchung eingeladen.3
Dennoch wird der Nutzen eines bevölkerungsweiten Mammographiescreenings bis heute kontrovers diskutiert,4-6 zum Teil mit schrillen Zügen: 2009 revidierte ein Expertengremium in den USA (U.S. Preventive Services Task Force) die bis dahin bestehende uneingeschränkte Empfehlung für ein routinemäßiges Screening 40- bis 49-jähriger Frauen aufgrund der in einer Metaanalyse gegenüber anderen Altersgruppen ungünstigeren Nutzen-Schaden-Relation. Für Frauen zwischen 50 und 74 Jahren wurde die uneingeschränkt positive Bewertung beibehalten. Das Gremium rät jedoch keineswegs grundsätzlich vom Screening jüngerer Frauen ab, sondern empfiehlt eine individuelle informierte Entscheidung unter Abwägen von Nutzen und Risiken7 - eine Empfehlung, die eigentlich selbstverständlich für alle zu beratenden Frauen gelten sollte. Die Folge waren nahezu hysterisch anmutende Kommentare.8 Die Autoren wurden von Befürwortern des Massenscreenings als "Idioten" bezeichnet.9 Ähnlich intensiv fielen die Reaktionen aus, als 2011 ein kanadisches Expertengremium (Canadian Task Force on Preventive Health Care) seine Empfehlungen zum Mammographiescreening in ähnlicher Form modifizierte.10,11 Den Mitgliedern des Gremiums wird in der Folge fehlerhafte Auswertung bzw. Ignorieren von Studienergebnissen und mangelnde Kompetenz vorgeworfen.12 Würde die geänderte Leitlinie befolgt, sei in Kanada mit dem zusätzlichen Tod von 2.000 Frauen in einem Zeitraum von zehn Jahren zu rechnen.13
MÖGLICHKEITEN UND GRENZEN VON SCREENING: Früherkennungsuntersuchungen haben zum Ziel, eine Krankheit in einem möglichst frühen Stadium zu erfassen, um die therapeutischen Möglichkeiten zu verbessern und die krankheitsbezogene Mortalität zu senken. Allerdings profitiert bei Weitem nicht jede Frau, bei der durch das Screening ein Brustkrebs diagnostiziert wird: Die Krankheit kann bei einem Teil der Betroffenen ebenso geheilt werden, wenn sie erst später in einem symptomatischen Stadium erfasst wird. Eine frühere durch das Screening induzierte Diagnose verlängert unter Umständen nicht das Leben, sondern lediglich die Zeitspanne, in der die Betroffene von ihrem Brustkrebs weiß, verbunden mit belastender Therapie. Auch kann es sein, dass die Krebserkrankung niemals klinisch manifest geworden wäre (Überdiagnose). Durch Screening werden zudem bevorzugt weniger aggressive Tumoren entdeckt, aggressiv wachsende häufig in Intervallen zwischen zwei Screeninguntersuchungen. Durch Mammographiescreening diagnostizierte Geschwülste zeigten in einer finnischen Studie gegenüber identisch großen klinisch erfassten eine geringere Neigung zur Fernmetastasierung.14 In einer US-amerikanischen Kohortenstudie zeigt sich ein deutlicher Trend zu gutartiger verlaufenden Tumoren, die im Screening erkannt werden.15
Der Intuition widersprechend, gehen Früherkennungsmaßnahmen immer mit Risiken einher, während die Vorteile erst gesichert werden müssen. Eine vorurteilsfreie Bewertung des Mammographiescreenings erfordert daher neben der Berücksichtigung des potenziellen Nutzens - Senkung der (krankheitsbedingten) Mortalität - auch eine Abschätzung des Schadens (falsch positive Befunde, Überdiagnostik/Übertherapie, Strahlenbelastung, Verängstigung der Teilnehmerinnen, falsche Sicherheit).
Wir hatten zuletzt 1999 eine Übersicht zum Datenstand des Mammographiescreenings gegeben (Sonderbeilage a-t 1999; Nr. 10). Seither ist eine Vielzahl von Auswertungen publiziert worden.
DATEN ZUR MORTALITÄTSSENKUNG: Die Erwartungen an Screeningprogramme waren von Beginn an sehr hoch, nachdem in den ersten randomisierten Studien16,17 eine 30%ige Senkung der Brustkrebsmortalität errechnet wurde. Diese Daten wurden durch metaanalytische Auswertung von vier schwedischen Studien unterstützt (Senkung um 29%).18 Senkungen der krankheitsspezifischen Mortalität um 50% wurden für die USA bis zum Jahr 2015 vorhergesagt.19 In einem regelmäßig aktualisierten systematischen Cochrane-Review1 errechnen die Autoren jedoch geringere Mortalitätssenkungen aus randomisierten kontrollierten Screeningstudien und üben zudem erhebliche Kritik an der methodischen Qualität der eingeschlossenen Arbeiten. Nur drei der acht Studien werden als angemessen randomisiert eingestuft. Für sieben gemeinsam ausgewertete Studien* wird eine Senkung der Sterblichkeit an Brustkrebs nach 7 und 13 Jahren um 19% errechnet. Bei Auswertung nur der drei Studien mit adäquater Randomisierung ergibt sich kein signifikanter Vorteil auf die krankheitsspezifische Mortalität (RR 0,93; 95% Konfidenzinterval [CI] 0,79-1,09). Die Krebssterblichkeit insgesamt wird nicht beeinflusst. Auch die Gesamtmortalität (Auswertung nur möglich anhand der drei adäquat randomisierten Studien) wird nicht signifikant gesenkt (nach sieben Jahren: RR 0,98; 95% CI 0,94-1,03; nach 13 Jahren: RR 0,99; 95% CI 0,95-1,03). Die Autoren geben zu bedenken, dass der in den Vordergrund gerückte Endpunkt, die krankheitsspezifische Mortalität, anfällig für Verzerrungen ist (die Festlegung auf eine Todesursache ist subjektiven Einflüssen unterworfen) und es konkrete Hinweise auf Fehlklassifizierungen gibt. Anders als zu erwarten wäre, sind zudem die Effekte in Studien mit schlechterem Equipment, großen Untersuchungsabständen und geringer Untersuchungszahl am größten, was ebenfalls als Indiz für Bias gedeutet wird.1
Für die Abschätzung des aktuellen Nutzens des Massenscreenings muss berücksichtigt werden, dass sich die Ergebnisse der zum größten Teil in den 1980er Jahren durchgeführten Studien aufgrund veränderter Umstände (verbesserte Therapieoptionen, zeitliche Verschiebungen des Eintritts von Menarche und Menopause, Rückgang der Anwendung von Hormontherapie im Klimakterium, größere Aufmerksamkeit der Frauen bezüglich Veränderungen der Brust) nicht ohne Weiteres auf die Gegenwart übertragen lassen. Zum Zeitpunkt der Durchführung der Studien war z.B. die adjuvante
Therapie mit Tamoxifen (NOLVADEX, Generika) kein Standard. Steigt die Überlebenswahrscheinlichkeit durch eine verbesserte Therapie, verringert sich der absolute Nutzen von Screeningmaßnahmen.20
Der in vielen Ländern beobachtete Rückgang der Brustkrebssterblichkeit ist nach epidemiologischen Arbeiten offenbar nicht allein auf das Screening zurückzuführen: In den Niederlanden wurde zwar der deutliche Rückgang der Krebssterblichkeit bei Frauen über 69 Jahren zwischen 1975 und 2006 als Erfolg des Screenings gefeiert.21 Der gleiche Trend war jedoch in dieser Altersgruppe auch in Norwegen und Irland zu sehen22 - ohne entsprechende Programme. Nach einer retrospektiven Analyse22 sinken die Sterblichkeitsraten an Brustkrebs von 1989 bis 2006 in Nordirland, den Niederlanden, Belgien, Schweden und Norwegen in gleichen Größenordnungen und zeitlich parallel um 20% bis 29%. In diesen Ländern wurden Screeningprogramme aber zu sehr unterschiedlichen Zeitpunkten eingeführt (Abstände von 10 bis 15 Jahren). Der Einfluss des Screenings auf die Brustkrebsmortalität wird daher als gering eingestuft.22 Daten aus Australien zeigen, dass zwischen 1991 und 2007 die Brustkrebsmortalität in allen untersuchten Altersstrata, auch in solchen, in denen kein Screening durchgeführt wurde, gleichermaßen sinkt. Die Autoren folgern, dass die moderne Chemotherapie und adjuvante endokrine Therapie wesentlich oder sogar allein für den positiven Trend verantwortlich sind.23 Die Etablierung von Tamoxifen in der adjuvanten Behandlung könnte der Grund dafür sein, dass die Brustkrebssterblichkeit bei jüngeren Frauen - bei denen häufiger Östrogenrezeptor-positive Tumoren vorliegen - stärker abnahm als bei älteren.24 Eine weitere retrospektive Analyse aus Norwegen errechnet zwar einen Rückgang der krankheitsspezifischen Mortalität zwischen 1996 (Einführung des bevölkerungsweiten Screenings) und 2005 um 7,2 Todesfälle/ 100.000 Personenjahre. Zwei Drittel dieser Reduktion (4.8/ 100.000) sind jedoch auch in der nicht gescreenten Population zu sehen.25 Eine Analyse US-amerikanischer Daten von 1975 bis 2000 schätzt den Anteil des Screenings an der Senkung der Brustkrebsmortalität je nach zu Grunde liegendem statistischen Modell zwischen 28% und 65%.26 Auswertungen aus Dänemark (Kopenhagen, Fünen) zeigen einen Rückgang der Brustkrebssterblichkeit in Gebieten mit Screening von 1%/Jahr, ohne Screening jedoch um 2%.27
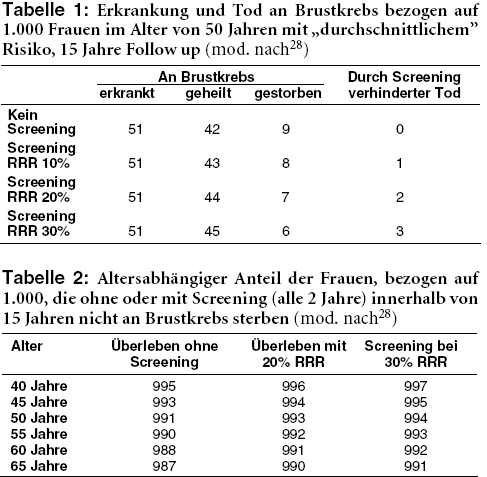
KOMMUNIKATION DES NUTZENS: In der Beratungssituation helfen die Angaben der relativen Risiken bzw. Risikoreduktionen der Brustkrebssterblichkeit wenig, da der überwiegende Teil der Frauen, die zum Screening eingeladen werden, gesund ist. Für die Frage, ob Brustkrebsscreening "mein Leben rettet", müssen die errechneten Zahlen in Bezug zur Gesamtheit der gescreenten Population gesetzt werden. Der hochgerechnete Nutzen für die einzelne Frau liegt auch bei unterschiedlichen Annahmen für die erzielten Risikoreduktionen nicht weit auseinander. Unter Berücksichtigung der Daten aus randomisierten kontrollierten Studien und der rückläufigen Brustkrebsmortalität aufgrund verbesserter Therapie werden nach einer Modellrechnung von 1.000 Frauen zwischen 50 und 65 Jahren, die 15 Jahre nachbeobachtet werden und nicht am Screening teilnehmen, neun an Brustkrebs sterben, unter Annahme einer 10%igen relativen Risikoreduktion durch Screening sind es acht. Bei Zugrundelegung einer 30%igen Risikoreduktion sind es sechs Frauen (siehe Tabelle 1).
Von der "anderen Seite" betrachtet, kann man die Wahrscheinlichkeit angeben, mit der eine Frau nicht an Brustkrebs stirbt (vgl. Tabelle 2). Dies macht deutlich, welcher Zugewinn an Sicherheit für die einzelne Frau durch Screening "herausspringt". So sterben beispielsweise von 1.000 50-jährigen Frauen ohne Screening 991 nicht an Brustkrebs, bei Zugrundelegung einer 30%-Risikoreduktion durch Screening sind es 994.
Nach einer aktuellen Analyse der kanadischen Task Force ist die Zahl der Frauen, die am Screening teilnehmen müssen, um einen Tod durch Brustkrebs zu verhindern (Number Needed to Screen [NNS]), zudem deutlich altersabhängig. Bei im Median elf Jahren Screening und vier Untersuchungen sind dies 2.108 Frauen (NNS) im Alter zwischen 40 und 49 Jahren, 721 zwischen 50 und 59 Jahren und 451 zwischen 70 und 74 Jahren.29
NEGATIVFOLGEN DES SCREENINGS: Wegen der schwerwiegenden Folgen werden Überdiagnosen als größter Nachteil des Massenscreenings angesehen. Überdiagnose ist die Feststellung einer Krebserkrankung, die im Laufe des Lebens klinisch nicht manifest geworden wäre und keinen Einfluss auf die Lebensspanne oder das Leiden der Betroffenen gehabt hätte. 30 Ursache ist langsames Tumorwachstum oder die Diagnose von grenzwertig malignen Veränderungen. Das Phänomen der Überdiagnostik kennt man auch bei anderen Karzinomen wie dem Prostatakarzinom (a-t 2009; 40: 33-4). Da in der Praxis nicht unterschieden werden kann, welcher Tumor einen gutartigen Verlauf nimmt, werden alle behandelt. Dies kann langsam-invasiv wachsende Tumoren betreffen. Seit Beginn der Screeningprogramme nimmt allerdings auch die Inzidenz des nicht tastbaren, bei der Mammographie jedoch durch Mikroverkalkungen auffälligen ductalen Carcinoma in situ (DCIS) deutlich zu, das vermutlich in weniger als der Hälfte der Fälle im Laufe des Lebens progredient verläuft.31 DCIS machen in Großbritannien 20%, in den USA 23%,32 hierzulande 20%33 der durch Screening entdeckten Brustkarzinome aus.
Zu Beginn jedes Screeningsprogramms steigt zunächst die Zahl der Diagnosen an. Diese sollte jedoch bei fehlender Überdiagnostik durch einen Rückgang nach Beendigung der Reihenuntersuchungen vollständig kompensiert werden, da die Diagnosestellung vorverlegt wurde, diese Erkrankungen also später nicht mehr inzident werden können. Bleibt die Inzidenz jedoch hoch, ist dies ein Hinweis auf Überdiagnosen. Eine frühe Berechnung aus einer der ersten randomisierten Studien, nach der das Problem quantitativ unerheblich sei und somit keine Rolle spiele, beruhte auf falscher Methodik.34 Aktuelle Analysen errechnen Überdiagnose-Raten zwischen 10% und 50%.1,35-38 Mitarbeiter des nordischen Cochrane-Zentrums schätzen, dass in Regionen, in denen Screening angeboten wird, eine von drei Brustkrebsdiagnosen eine Überdiagnose darstellt.38 Überdiagnostik führt zu unnötiger (Über-)Therapie, die mit den üblichen Risiken einer Krebstherapie verbunden ist. Neben den Risiken operativer Eingriffe, der Chemo- und endokrinen Therapie kann sich auch unnötige Strahlentherapie durch kardiale Folgeerkrankungen und erhöhtes Lungenkrebsrisiko negativ auswirken.34 Durch Einführung verfeinerter Diagnosemethoden wird das Problem der Überdiagnostik vermutlich weiter verschärft.
Als zusätzlicher Nutzen für das Massenscreening wird behauptet, dass die Mastektomierate wegen der früheren Diagnose halbiert wird.39 Dies wird auch für das Programm in Deutschland in Anspruch genommen: Durch die häufigere Entdeckung kleiner Tumoren ließen sich eingreifende therapeutische Maßnahmen vermeiden.33 Dabei wird jedoch außer Acht gelassen, dass insgesamt die Zahl invasiver Eingriffe, inklusive Mastektomien, nicht zuletzt als Folge der Überdiagnostik, zunimmt. Insgesamt erhöht sich die Mastektomierate in den gescreenten Populationen relativ um 20%.1
Falsch positive Befunde, also auffällige Befunde in der Mammographie, die sich als "Fehlalarm" herausstellen, führen zu erheblicher Besorgnis und psychischem Stress bei der betroffenen Frau, die auch nach Ausräumen eines Verdachtes anhalten können.40,41 Hinzu kommen weitere diagnostische Schritte zur Abklärung, ggf. verbunden mit zusätzlicher Strahlenbelastung. Bei einem Teil folgen invasive Maßnahmen durch chirurgische oder perkutane Biopsie. Im schlimmsten Fall wird unnötig operiert. Das Ausmaß der falsch positiven Befunde ist erheblich: Nach retrospektiven Daten einer Kohortenstudie mit 2.400 Frauen zwischen 40 und 69 Jahren wurde nach im Median vier Mammographien im Verlauf von zehn Jahren bei 24% der teilnehmenden Frauen mindestens ein falsch positiver Befund erhoben. Die Autoren rechnen hoch, dass nach zehn Mammographien - dies entspricht der Anzahl der im deutschen Programm pro Frau vorgesehenen Untersuchungen - bei 49% der Teilnehmerinnen mindestens ein falsch positiver Befund zu erwarten ist.42
In einer aktuellen Metaanalyse wird die Zahl falsch positiver Befunde nach Daten aus Kanada hochgerechnet. Auch nach dieser Auswertung ergeben sich im Verlauf von vier Mammographien falsch-positive Befunde bei jeder dritten bis fünften Frau (Tabelle 3).

Im deutschen Programm liegt die Rate falsch-positiver Befunde im Zeitraum 2008 bis 2009, entsprechend einer Screeningrunde, bei 4,6%.33
In welchem Umfang die diagnostische Strahlenbelastung zu zusätzlichen Brustkrebserkrankungen führt, ist nur durch komplexe Modellrechnungen zu evaluieren, wobei große Unsicherheiten bestehen. Die Gefährdung betrifft eher jüngere Frauen, da die Strahlensensibilität des Brustgewebes mit dem Alter abnimmt. Eine Hochrechnung aus dem Jahr 1996 schätzt, dass bei regelmäßiger Mammographie ab dem 40. Lebensjahr mit 1,5 bis 4,5 zusätzlichen Brustkrebserkrankungen/10.000 Frauen zu rechnen ist.43 Neuere Berechnungen geben an, dass in Abhängigkeit von dem zu Grunde gelegten Modell auf 84 bis 2.200 durch Mammographiescreening entdeckte Brustkarzinome 1 durch die Bestrahlung induzierter Tumor kommt.44
INFORMATIONSSCHRIFTEN: Die europäische Leitlinie45 zur Kommunikation mit den Frauen sieht vor, dass die Informationen umfassend sein und nicht einseitig zur Teilnahme motivieren sollen. "Die Informationen sollten unbedingt ausgewogen sein, das heißt, sie informieren auch über Risiken
"45 Dennoch wird die mangelnde Qualität der offiziell zur Verfügung gestellten Informationsschriften zum Mammographiescreening zum Teil scharf kritisiert.46 Der Nutzen werde darin zu einseitig dargestellt, ohne auf Schädigungsaspekte einzugehen. Tauchten diese auf, seien sie so verklausuliert, dass sie kaum zu verstehen seien und sogar als Nutzen fehlgedeutet werden könnten.
In Deutschland wird mit dem 2010 vom Gemeinsamen Bundesausschuss (G-BA) zusammen mit der Kooperationsgemeinschaft Mammographie aufgelegten Informationsblatt zwar auf Einschränkungen und Nachteile des Screenings eingegangen.47 Ob jedoch Frauen den Satz "Von diesen 10 Frauen (mit Diagnose Brustkrebs aufgrund des Screenings, -Red.) hätte eine Frau ohne Mammographie zu Lebzeiten nichts von ihrem Brustkrebs erfahren
" als Quantifizierung der Überdiagnostik begreifen, ist anzuzweifeln. Alternative Informationsbroschüren des Nationalen Netzwerk Frauen und Gesundheit48 oder des nordischen Cochrane-Zentrums49 erscheinen demgegenüber in Sprache und Darstellung klarer und verständlicher. Auch die hierzulande an die Frauen versandten Einladungen zum Screening erachten wir als problematisch. Zwar werden die positiven Ziele der Reihenuntersuchung erwähnt, ein Hinweis auf Nachteile fehlt jedoch. Die eingeladene Frau wird lediglich auf die im Internet verfügbare Informationsschrift verwiesen. Zudem werden Frauen mit dem schon im gleichen Schreiben angebotenen Untersuchungstermin unter Druck gesetzt.50
Obgleich in Deutschland und in vielen anderen Ländern Programme zum Mammographiescreening auf Brustkrebs etabliert sind, wird über Nutzen und Risiken des Screenings kontrovers diskutiert. Die Hinweise auf eine Senkung der Brustkrebssterblichkeit stammen überwiegend aus alten, methodisch angreifbaren Studien, die den Effekt des Screenings überschätzen dürften.
Der in vielen Ländern anhaltende Trend zu einer verringerten Brustkrebssterblichkeit scheint vorwiegend auf andere Faktoren wie verbesserte Therapiemöglichkeiten zurückzuführen zu sein.
Dem möglichen Nutzen einer verminderten Brustkrebsmortalität stehen Risiken gegenüber. Insbesondere Überdiagnostik und dadurch bedingte Übertherapie sind gravierende Nachteile. Zudem müssen bis zu 50% der Frauen bei zehn Screeningrunden mit mindestens einem Fehlalarm rechnen.
Frauen, die zum Screening eingeladen werden, müssen ihre Entscheidung für oder gegen die Untersuchung ohne Druck und auf Grundlage vollständiger Informationen zu Nutzen und Risiken treffen können. Diesbezüglich besteht auch hierzulande Verbesserungsbedarf.
| (R =randomisierte Studie, M = Metaanalyse) | |
| M 1 | GØTZSCHE, P.C., NIELSEN, M.: Screening for breast cancer with mammography. The Cochrane Database of Systematic Reviews 2011; Stand Nov. 2008, Zugriff März 2012 |
| 2 | SHAPIRO, S. et al.: Int. J. Epidemiol. 1998; 27: 735-42 |
| 3 | Gemeinsamer Bundesausschuss: Änderung der Krebsfrüherkennungs-Richtlinie vom 15.12.2003; http://www.g-ba.de/downloads/39-261-33/2003-12-15-Krebs-Mammo.pdf |
| 4 | JØRGENSEN, K.J. et al.: Radiology 2011; 260: 621-7 |
| 5 | GØTZSCHE, P.C. et al.: BMJ 2009; 338: b86 (3 Seiten) |
| 6 | WALD, N.J. et al.: BMJ 2009; 339: b2922 (1 Seite) |
| 7 | US Preventive Services Task Force: Ann. Intern. Med. 2009; 151: 716-26 |
| 8 | KOPANS, D.B.: Radiol. Clin. North Am. 2010; 48: 843-57 |
| 9 | KAMEROW, D.: BMJ 2009; 339: b5175 (4 Seiten) |
| 10 | O'DOWD, A.: BMJ 2011; 343: d7625 (1 Seite) |
| 11 | TONELLI, M. et al.: CMAJ 2011; 183: 1991-2001 |
| 12 | YAFFE, M.: Why I reject most of the new breast cancer screening recommondations; zu finden unter: http://www.theglobeandmail.com |
| 13 | cbc news/health: 2011; Breast cancer screening guide says skip exams http://www.cbc.ca/news/health/story/2011/11/21/breast-cancer-screening.html |
| 14 | JOENSUU, H. et al.: JAMA 2004; 292: 1064-73 |
| 15 | MALMGREN, J.A. et al.: BMC. Cancer 2008; 8: 131 (7 Seiten) |
| R 16 | ARON, J.L., PROROK, P. C.: Int. J. Epidemiol. 1986; 15: 36-43 |
| R 17 | SHAPIRO, S. et al.: J. Natl. Cancer Inst. 1982; 69: 349-55 |
| M 18 | NYSTROM, L. et al.: Lancet 1993; 341: 973-8 |
| 19 | BYERS,T. et al.: Cancer, 1999; 86: 715-27 |
| 20 | GLASZIOU, P., HOUSSAMI, N.: Preventive Medicine 2011; 53: 100-2 |
| 21 | OTTEN, J.D. et al.: Int. J. Cancer 2008; 123: 1929-34 |
| 22 | AUTIER, P. et al.: BMJ 2011; 343: d4411 |
| 23 | BURTON, R.C. et al.: Breast Cancer Res. Treat. 2012; 131: 949-55 |
| 24 | GØTZSCHE, P.C.: CMAJ 2011; 183: 1957-8 |
| 25 | KALAGER, M. et al.: N. Engl. J. Med. 2010; 363: 1203-10 |
| 26 | BERRY, D.A. et al.: N. Engl. J. Med. 2005; 353: 1784-92 |
| 27 | JØRGENSEN, K.J. et al.: BMJ 2010; 340: c1241 (6 Seiten) |
| 28 | KEEN, J.D., KEEN, J.E.: BMC. Med. Inform. Decis. Mak. 2009; 9: 18 (14 Seiten) |
| 29 | FITZPATRICK-LEWIS, D. et al.: Breast Cancer Screening, Stand Okt. 2011; http://www.canadiantaskforce.ca/docs/breast_cancer_2011_systematic_review_ENG.pdf |
| 30 | WELCH, H.G., BLACK, W.C.: J. Natl. Cancer Inst. 2010; 102: 605-13 |
| 31 | WELCH, H.G. et al.: BMJ 2009; 339: b1425 |
| 32 | U.S. Preventive Task Force 2009: Screening for Breast Cancer: Systematic Evidence Review Update for the U.S. Preventive Services Task Force http://www.uspreventiveservicestaskforce.org/uspstf09/breastcancer/brcanes.pdf |
| 33 | Evaluationsbericht 2008-2009; Ergebnisse des Mammographie-Screening-Programms in Deutschland, Februar 2012; http://www.mammo-programm.de/cms_upload/fck-userfies/Evaluations bericht_2008-2009_web.pdf Zugriff März 2012 |
| 34 | JØRGENSEN, K.J. et al.: Radiology 2011; 260: 621-7 |
| 35 | ZACKRISSON, S. et al.: BMJ 2006; 332: 689-92 |
| 36 | WELCH, H.G., BLACK, W.C.: J. Natl. Cancer Inst. 2010; 102: 605-13 |
| 37 | JØRGENSEN, K.J. et al.: BMC. Womens Health 2009; 9: 36 |
| 38 | JØRGENSEN, K.J., GØTZSCHE, P.C.: BMJ 2009; 339: b2587 |
| 39 | BOCK, K. et al.: Lancet 2011; 378: 1775-6 |
| 40 | GRAM, I.T. et al.: Br. J. Cancer 1990; 62: 1018-22 |
| 41 | LERMAN, C. et al.: Ann.Intern.Med. 1991; 114: 657-61 |
| 42 | ELMORE, J.G. et al.: N. Engl. J. Med. 1998; 338: 1089-96 |
| 43 | METTLER, F.A. et al.: Cancer 1996; 77: 903-9 |
| 44 | LAW, J. et al.: Br. J. Radiol. 2007; 80: 261-6 |
| 45 | Kooperationsgemeinschaft Mammographie : Übersetzung des Kapitels 12 der Europäischen Leitlinien für Qualitätssicherung des Brustkrebs-Screenings; http://www.mammo-programm.de/cms:upload/fck-userfies/broschuere_eu_guideline_internet.pdf |
| 46 | GØTZSCHE, P.C. und GØRGENSEN, K.S. : J. R. Soc. Med. 2011; 104: 361-9 |
| 47 | Gemeinsamer Bundesausschuss : Informationen zum Mammographie-Screening, Stand Juni 2010; zu finden unter http://www.mammo-programm.de/startseite/startseite.php |
| 48 | Nat. Netzwerk Frauen und Gesundheit: Brustkrebs Früherkennung, Stand Jan. 2006 |
| 49 | GØTZSCHE, P.C. et al.: Informationsschrift: Screening for breast cancer with mammography, Stand Jan. 2012 http://www.cochrane.dk/screening/mammography-leaflet.pdf |
| 50 | Kooperationsgemeinschaft Mammographie: Mustereinladungsschreiben, Stand Juli 2011; http://www.mammo-programm.de/cms_upload/datenpool/mustereinladungsschreiben_stand_juli_2011.pdf |
| R 51 | ALEXANDER, F.E. et al.: Lancet 1999; 353: 1903-8 |
| * | Eine der Studien51 wird wegen zu großer Verzerrungsgefahr nur gesondert dargestellt. |
© 2012 arznei-telegramm, publiziert am 9. März 2012
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
