|
"Nebenwirkungen ... auf Plazebo-Niveau"1 wurden dem oralen Antidiabetikum Troglitazon bei Markteinführung in den USA (REZULIN)
bescheinigt (a-t 1997; Nr. 12: 127).1,2 Inzwischen ist es wegen Lebertoxizität mit mindestens 63
Todesfällen3 weltweit aus dem Verkehr. SmithKline Beecham bringt jetzt die Molekülvariante Rosiglitazon (AVANDIA) als "sehr gut
verträglich" in den Handel. Das Mittel soll die Insulinresistenz ursächlich vermindern; Werbung: "Insulinresistenz: Es gibt ein Zurück!
"4
Das Thiazolidindion Rosiglitazon ist ausschließlich als Zusatz zur Behandlung des Typ-2-Diabetes bei nicht ausreichender Wirksamkeit von Sulfonylharnstoffen
oder dem Biguanid Metformin (GLUCOPHAGE u.a.) zugelassen.5 Als Monotherapeutikum schneidet Rosiglitazon im einjährigen
(unveröffentlichten!) Vergleich schlechter ab als Glibenclamid (EUGLUCON N u.a.).6,7 Der Antrag auf Zulassung zur Monotherapie wurde vom
Europäischen Arzneimittelausschuss CPMP abgelehnt.8
KLINISCHE STUDIEN: Zwei halbjährige plazebokontrollierte Phase-III-Studien mit 350 und 590 Patienten liegen veröffentlicht vor. Als Zusatz zu
Sulfonylharnstoffen oder hochdosiertem Metformin (2,5 g/Tag) senkt Rosiglitazon das HbA1c dosisabhängig um 0,6% bis 1,2%. In Kombination mit
Sulfonylharnstoffen wurden täglich 2 mg bzw. 4 mg Rosiglitazon geprüft, bei Metformin-Einnahme täglich 4 mg bzw. 8 mg. Die
Untersuchungsergebnisse stammen aus Labors des Herstellers SmithKline Beecham.9,10 Klinische Endpunkte sind nicht geprüft.
BEDENKLICHE EFFEKTE UND TOXIZITÄT: Mit der Werbung "sehr gut verträglich"4 verharmlost SmithKline Beecham das
bedenkliche Schädigungspotenzial von Rosiglitazon. Verschiedene Organsysteme können betroffen sein:
 Gewicht: Glitazone sollen die Insulinresistenz bei Diabetes beeinflussen - wie,
ist nicht vollständig geklärt. Entscheidender Effekt scheint jedoch die Vermehrung von Fettgewebe durch Aktivierung eines Zellkernrezeptors (PPAR-(*) zu
sein.11 Die neu entstehenden Fettzellen nehmen Blutglukose auf und speichern sie als Fett. Der Wirkmechanismus hat regelmäßig eine
unerwünschte Folge: Das Körpergewicht steigt. In klinischen Studien mit Rosiglitazon zeichnet sich eine kontinuierliche Gewichtszunahme ab, ohne
Hinweis auf Stopp.7 Sie beträgt innerhalb eines halben Jahres durchschnittlich 4% bis 6% des Ausgangsgewichts.5 Nach dem, was man aus
humangenetischen und tierexperimentellen Studien weiß, ist damit zu rechnen, dass ab einer kritischen Schwelle der Fettgewebsvermehrung die
Insulinresistenz wieder zunimmt.11 Der Langzeitnutzen der Behandlung ist daher fraglich. Gewicht: Glitazone sollen die Insulinresistenz bei Diabetes beeinflussen - wie,
ist nicht vollständig geklärt. Entscheidender Effekt scheint jedoch die Vermehrung von Fettgewebe durch Aktivierung eines Zellkernrezeptors (PPAR-(*) zu
sein.11 Die neu entstehenden Fettzellen nehmen Blutglukose auf und speichern sie als Fett. Der Wirkmechanismus hat regelmäßig eine
unerwünschte Folge: Das Körpergewicht steigt. In klinischen Studien mit Rosiglitazon zeichnet sich eine kontinuierliche Gewichtszunahme ab, ohne
Hinweis auf Stopp.7 Sie beträgt innerhalb eines halben Jahres durchschnittlich 4% bis 6% des Ausgangsgewichts.5 Nach dem, was man aus
humangenetischen und tierexperimentellen Studien weiß, ist damit zu rechnen, dass ab einer kritischen Schwelle der Fettgewebsvermehrung die
Insulinresistenz wieder zunimmt.11 Der Langzeitnutzen der Behandlung ist daher fraglich.
 Leber: Leberschäden, die zur Marktrücknahme von Troglitazon
geführt haben, kommen auch unter Einnahme von Rosiglitazon vor. Ein Klasseneffekt wird diskutiert.7,12 Leberversagen mit tödlichem Verlauf ist
beschrieben.5 Wenn ein herstellernaher2 Meinungsbildner heute noch öffentlich behauptet, es seien "keine schwerwiegenden
unerwünschten Effekte und ... keine Lebertoxizität gemeldet worden"13, kann dies - ebenso wie die AVANDIA-Werbung - nur als gezielte
Desinformation gewertet werden. In den ersten vier Monaten nach Markteinführung im Juni 1999 erhielt die US-amerikanische Arzneimittelbehörde FDA
vier Berichte über Leberversagen unter Rosiglitazon.7 Zwei Berichte über Leberversagen und schwere Leberschädigung sind seit Januar
2000 publiziert.14,15 Dass die regelmäßige Überwachung der Leberwerte Anwender vor lebensbedrohlicher Schädigung bewahrt, ist
nach den Erfahrungen mit Troglitazon nicht zu erwarten. Leber: Leberschäden, die zur Marktrücknahme von Troglitazon
geführt haben, kommen auch unter Einnahme von Rosiglitazon vor. Ein Klasseneffekt wird diskutiert.7,12 Leberversagen mit tödlichem Verlauf ist
beschrieben.5 Wenn ein herstellernaher2 Meinungsbildner heute noch öffentlich behauptet, es seien "keine schwerwiegenden
unerwünschten Effekte und ... keine Lebertoxizität gemeldet worden"13, kann dies - ebenso wie die AVANDIA-Werbung - nur als gezielte
Desinformation gewertet werden. In den ersten vier Monaten nach Markteinführung im Juni 1999 erhielt die US-amerikanische Arzneimittelbehörde FDA
vier Berichte über Leberversagen unter Rosiglitazon.7 Zwei Berichte über Leberversagen und schwere Leberschädigung sind seit Januar
2000 publiziert.14,15 Dass die regelmäßige Überwachung der Leberwerte Anwender vor lebensbedrohlicher Schädigung bewahrt, ist
nach den Erfahrungen mit Troglitazon nicht zu erwarten.
 Herz/Kreislauf: Im Tierversuch wirken alle Thiazolidindione kardiotoxisch.
Myokardinfarkte kommen in klinischen Studien unter Rosiglitazon insgesamt offenbar häufiger vor als in Kontrollgruppen.7 Das Mittel potenziert zudem
einen Mechanismus,16 durch den Sulfonylharnstoffe die Ausbildung einer Ischämietoleranz (so genannte ischämische Präkonditionierung)
blockieren. Es dürfte somit deren Kardiotoxizität verstärken. Schließlich verursachen Glitazone Wassereinlagerung, die eine Herzinsuffizienz
auslösen oder verschlechtern kann. Die FDA verzeichnet innerhalb von 19 Monaten 56 Berichte über Herzinsuffizienz unter Troglitazon. Zu Rosiglitazon
liegen nach vier Monaten fünf Berichte vor.7 Wegen gehäufter Herzinsuffizienz bei Komedikation mit Insulin ist diese Kombination
kontraindiziert.5 Ödeme betreffen 5% der Rosiglitazon-Anwender.12 Unter Troglitazon ist Lungenödem beschrieben. Herz/Kreislauf: Im Tierversuch wirken alle Thiazolidindione kardiotoxisch.
Myokardinfarkte kommen in klinischen Studien unter Rosiglitazon insgesamt offenbar häufiger vor als in Kontrollgruppen.7 Das Mittel potenziert zudem
einen Mechanismus,16 durch den Sulfonylharnstoffe die Ausbildung einer Ischämietoleranz (so genannte ischämische Präkonditionierung)
blockieren. Es dürfte somit deren Kardiotoxizität verstärken. Schließlich verursachen Glitazone Wassereinlagerung, die eine Herzinsuffizienz
auslösen oder verschlechtern kann. Die FDA verzeichnet innerhalb von 19 Monaten 56 Berichte über Herzinsuffizienz unter Troglitazon. Zu Rosiglitazon
liegen nach vier Monaten fünf Berichte vor.7 Wegen gehäufter Herzinsuffizienz bei Komedikation mit Insulin ist diese Kombination
kontraindiziert.5 Ödeme betreffen 5% der Rosiglitazon-Anwender.12 Unter Troglitazon ist Lungenödem beschrieben.
 Blutfette: Gesamtcholesterin, LDL und HDL steigen unter der Einnahme
an.9,10 Auch der LDL/HDL-Quotient scheint zuzunehmen.7 Die langfristigen Auswirkungen von Gewichtszunahme und Hyperlipidämie
hinsichtlich kardiovaskulärer Folgeerkrankungen sind nicht bekannt. Blutfette: Gesamtcholesterin, LDL und HDL steigen unter der Einnahme
an.9,10 Auch der LDL/HDL-Quotient scheint zuzunehmen.7 Die langfristigen Auswirkungen von Gewichtszunahme und Hyperlipidämie
hinsichtlich kardiovaskulärer Folgeerkrankungen sind nicht bekannt.
 Blut: Anämie (2%, bei Kombination mit Metformin 7%6) und Leukopenie
dürften nicht allein auf erhöhtem Plasmavolumen beruhen. Als Auslöser kommen Verdrängung von Knochenmarkzellen durch Fettzellen oder
auch direkte Störung der Stammzellen im Knochenmark durch Glitazone in Betracht.7 Blut: Anämie (2%, bei Kombination mit Metformin 7%6) und Leukopenie
dürften nicht allein auf erhöhtem Plasmavolumen beruhen. Als Auslöser kommen Verdrängung von Knochenmarkzellen durch Fettzellen oder
auch direkte Störung der Stammzellen im Knochenmark durch Glitazone in Betracht.7
 Hormone: Rosiglitazon hemmt ein Schlüsselenzym der Steroidsynthese.
Bei weiblichen Affen setzt der Eisprung aus.7 Andererseits soll sich eine durch Insulinresistenz bedingte Anovulation unter der Einnahme zurückbilden.
Bei Eintritt einer Schwangerschaft ist die Behandlung abzubrechen. Im Tierversuch wirkt das Mittel fetotoxisch.5 Hormone: Rosiglitazon hemmt ein Schlüsselenzym der Steroidsynthese.
Bei weiblichen Affen setzt der Eisprung aus.7 Andererseits soll sich eine durch Insulinresistenz bedingte Anovulation unter der Einnahme zurückbilden.
Bei Eintritt einer Schwangerschaft ist die Behandlung abzubrechen. Im Tierversuch wirkt das Mittel fetotoxisch.5
 Tumorigenität: Im Tierversuch lösen Glitazone Darmtumoren aus.
Menschen mit familiärer adenomatöser Polyposis coli sollen die Mittel nicht einnehmen.11 Tumorigenität: Im Tierversuch lösen Glitazone Darmtumoren aus.
Menschen mit familiärer adenomatöser Polyposis coli sollen die Mittel nicht einnehmen.11
KOSTEN: Rosiglitazon (AVANDIA) kostet monatlich 94 DM (4 mg/Tag) bis 143 DM (8 mg/Tag). Die Zusatztherapie verteuert die Behandlung mit
Glibenclamid- oder Metformin-Nachfolgepräparaten um das 15fache (bei 8,75 mg Glibenclamid + 4 mg Rosiglitazon) bzw. um das 4-6fache (bei 2550 mg
Metformin + 4-8 mg Rosiglitazon).

FAZIT: Bei dem neuen oralen Antidiabetikum Rosiglitazon (AVANDIA) handelt es sich unseres Erachtens um ein bedenkliches Arzneimittel. Das Mittel kann
lebensbedrohliche Herzinsuffizienz und - wie der inzwischen weltweit abgestürzte Vorläufer Troglitazon - Leberversagen auslösen. Bei Kombination
mit Sulfonylharnstoffen wie Glibenclamid (EUGLUCON u.a.) dürften deren kardiotoxische Wirkungen verstärkt werden. Das Körpergewicht der
ohnehin häufig übergewichtigen Patienten und die Blutfette steigen an. Mit Ödemen und Anämie ist zu rechnen. Diesen gefährlichen
Risiken steht kein adäquater Nutzen gegenüber.
Die Werbung für Rosiglitazon - "sehr gut verträglich"3 - führt verordnende Ärzte und Patienten gezielt in die Irre. Die Marktzulassung
eines derartigen Produktes können wir nicht nachvollziehen.
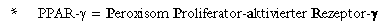

|


