LIPASEHEMMER ORLISTAT ALS ALLI JETZT REZEPTFREI
Der Lipasehemmer Orlistat (XENICAL, a-t 1998; Nr. 9: 77-8) wird seit April in halber Dosierung als "ALLI" rezeptfrei angeboten. ALLI ist für die Gewichtsreduktion von Erwachsenen mit Body-Mass-Index von mindestens 28 kg/m2 zugelassen und soll nicht länger als sechs Monate eingenommen werden.1 Flankiert wird die Einführung von einer groß angelegten Marketingkampagne, die erahnen lässt, was auf uns zukäme, wenn das Verbot der "Direct-to-Consumer"-Werbung für rezeptpflichtige Arzneimittel, das für das rezeptfreie ALLI nicht gilt, in der EU aufgehoben würde.

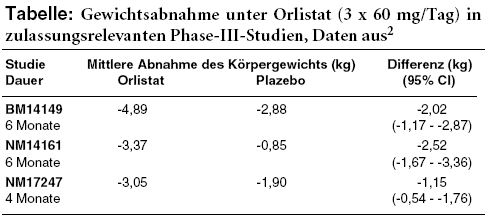
KLINISCHE WIRKSAMKEIT: In zwei zulassungsrelevanten Phase-III-Studien mit insgesamt knapp 1.400 Teilnehmern, deren Body-Mass-Index (BMI) zu Studienbeginn zwischen 28 kg/m2 und 43 kg/m2 liegt, geht das Körpergewicht unter der ALLI-Dosierung von dreimal täglich 60 mg innerhalb von sechs Monaten im Mittel um 2 kg bis 2,5 kg stärker zurück als unter Plazebo (siehe Tabelle). In einer dritten viermonatigen Studie mit knapp 400 schlankeren Teilnehmern, deren BMI zwischen 25 kg/m2 und 28 kg/m2 liegt und für die das Mittel nicht zugelassen wurde, beträgt die mittlere Differenz bei Studienende nur 1,2 kg. Basis der Behandlung ist in allen drei Studien eine hypokalorische Diät.2,4-6
Wird Orlistat abgesetzt, nimmt das Gewicht wieder zu. In einer von zwei plazebokontrollierten Studien mit XENICAL (3 x täglich 120 mg), in denen ein Teil der Verumgruppe nach einem Jahr randomisiert auf Plazebo wechselt, unterscheidet sich der Gewichtsverlust unter dieser Strategie nach einem weiteren Jahr nicht von dem derjenigen Teilnehmer, die die ganze Zeit nur Plazebo eingenommen haben.2,7 Auch in der zweiten Studie wird ein "deutlicher Reboundeffekt" beobachtet.8 Entsprechende Daten finden wir für ALLI nicht. Aber selbst wenn Orlistat weiter eingenommen wird, steigt das Gewicht in plazebokontrollierten Studien ab dem zweiten Anwendungsjahr graduell wieder an.2,9 Ein klinischer Nutzen von Orlistat über die kurzfristige und geringfügige Gewichtsabnahme hinaus ist nicht belegt.10
UNERWÜNSCHTE WIRKUNGEN: Erwartungsgemäß dominieren gastrointestinale Störwirkungen. Sehr häufig (bei mindestens 10%) kommen fettiger öliger Stuhl, Abgang öliger Flüssigkeit, Flatulenz und Flatulenz mit Stuhlabgang vor, häufig (bei 1% bis 10%) flüssige Stühle, Stuhlinkontinenz und Unterbauchschmerzen.1 In den USA rät der Hersteller ALLI-Anwendern, dunkle Hosen zu tragen und Kleidung zum Wechseln mit zur Arbeit zu nehmen.11*
| * | O-Ton: "You may feel an urgent need to go to the bathroom. Until you have a sense of any treatment effects, it's probably a smart idea to wear dark pants, and bring a change of clothes with you to work."11 |
Mit dem Fett hemmt Orlistat auch die Absorption von fettlöslichen Vitaminen und Arzneimitteln. Abstoßungsreaktionen bei Komedikation mit Ciclosporin A (SANDIMMUN, Generika) und Krampfanfälle bei gleichzeitiger Einnahme von Antiepileptika sind beschrieben.2,3 Eine kontraindizierte Selbstmedikation mit ALLI z.B. bei Transplantatempfängern könnte zum Transplantatverlust führen.
Nach Markteinführung von Orlistat als XENICAL wurde über Cholelithiasis, Hepatitis, Pankreatitis, rektale Blutungen, Oxalatnephropathie und Überempfindlichkeitsreaktionen berichtet.3 In einer plazebokontrollierten Studie mit 539 Jugendlichen wurde eine erhöhte Frakturrate unter XENICAL gefunden (6% vs. 2,8%).3 Ein Hinweis darauf fehlt in der Publikation.12 Die in Zulassungsstudien beobachtete Häufung von Brustkrebs unter XENICAL wurde in weiteren Phase-III-Studien von ähnlichem Umfang, die der Hersteller vor Zulassung in den USA einreichen musste, nicht mehr beobachtet. Da in Tierversuchen zudem keine Zunahme festgestellt wurde und Orlistat kaum systemisch wirkt, stuft die US-amerikanische Arzneimittelbehörde FDA den Befund als zufallsbedingt ein.13
KOSTEN: Eine ALLI-Packung mit 84 Kapseln - ausreichend für 4 Wochen - kostet 59,90 € (in Österreich 64,50 €).
Der jetzt rezeptfrei als ALLI vermarktete Lipasehemmer Orlistat (rezeptpflichtig: XENICAL) senkt das mittlere Körpergewicht in den zugelassenen sechs Anwendungsmonaten geringfügig um zwei bis zweieinhalb Kilogramm.
Nach Absetzen von Orlistat steigt das Gewicht wieder an. Ein Jahr nach Absetzen selbst der doppelt so hohen XENICAL-Dosis ist in einer von zwei Studien kein Vorteil gegenüber Plazebo mehr zu erkennen.
Unangenehme und beschämende Störwirkungen wie Stuhlinkontinenz oder Blähungen mit Stuhlabgang sind häufig oder sehr häufig.TEXT
Fehlanwendungen, zum Beispiel bei Transplantatempfängern, können lebensbedrohlich sein.
Das Geld und die unangenehmen Erfahrungen mit ALLI kann man sich sparen: Nicht kaufen!
| (R = randomisierte Studie) | ||
| 1 | GlaxoSmithKline: Fachinformation ALLI, Stand März 2009 | |
| 2 | FDA/CDER: Medical Review Orlistat (ALLI), 2007; zu finden über: http://www.fda.gov/cder/foi/nda/2007/021887s000TOC.htm | |
| 3 | EMEA: Europ. Beurteilungsber. (EPAR) XENICAL, Stand Mai 2009; http://www.emea.europa.eu/humandocs/Humans/EPAR/xenical/xenical.htm | |
| 4 | EMEA: Europ. Beurteilungsbericht (EPAR) ALLI, Stand April 2009; http://www.emea.europa.eu/humandocs/Humans/EPAR/alli/alli.htm | |
R |
5 | ANDERSON, J.W. et al.: Ann. Pharmacother. 2006; 40: 1717-23 |
| R | 6 | HAUPTMAN, J. et al.: Arch. Fam. Med. 2000; 9: 160-7 |
| R | 7 | DAVIDSON, M.H. et al.: JAMA 1999; 281: 235-42 |
| R | 8 | SJÖSTRÖM, L. et al.: Lancet 1998; 352: 167-73 |
| R | 9 | TORGERSON, J.S. et al.: Diabetes Care 2004; 27: 155-61 |
| 10 | La Revue Prescrire 2009; 29: 175 | |
| 11 | GlaxoSmithKline: Werbung für ALLI, 2009 http://www.myalli.com/howdoesitwork/treatmenteffects.aspx | |
| 12 | CHANOINE, J.-P. et al.: JAMA 2005; 293: 2873-83 | |
| 13 | FDA: Schreiben vom 7. Feb. 2007; http://www.fda.gov/ohrms/dockets/dockets/06p0154/06P-0154-pdn0001.pdf |
© 2009 arznei-telegramm, publiziert am 15. Mai 2009
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
