ANTIARRHYTHMIKUM DRONEDARON (MULTAQ) BEI VORHOFFLIMMERN
Bei Vorhofflimmern gilt nach wie vor die Strategie der Frequenzkontrolle mit adäquater Antikoagulation als Verfahren der Wahl.1 Durch kontrollierte Studien ist bisher nicht bewiesen, dass eine Rhythmuskontrolle der Frequenzkontrolle im Hinblick auf Mortalität und Morbidität überlegen ist (a-t 2008; 39: 76, 2003; 34: 2-3). Soll jedoch eine Rhythmuskontrolle erreicht werden, gilt Amiodaron (CORDAREX, Generika) als wirksamstes Medikament.1,2 Eine langfristige Einnahme wird aber durch häufige Störwirkungen limitiert, vor allem an Haut, Schilddrüse, peripheren Nerven und Lunge.3 Mit Dronedaron (MULTAQ) wurde Ende 2009 im zweiten Anlauf ein Amiodaronanalog ohne Jod-Substituenten zur Rezidivprophylaxe bei nichtpermanentem Vorhofflimmern und zur Kontrolle der Ventrikelfrequenz zugelassen.4,5 2006 hatte ein Antrag weder in den USA noch in der EU vornehmlich wegen Sicherheitsbedenken Bestand.5,6
EIGENSCHAFTEN: Dronedaron ist wie Amiodaron ein Benzofuranderivat, jedoch weniger lipophil. Es wird geringer im Gewebe angereichert und rascher eliminiert. Seine elektrophysiologischen Effekte sind komplex und lassen keine Einordnung in die Klassifikation nach VAUGHAN-WILLIAMS zu. Es hemmt hauptsächlich den Kalium-Ausstrom, aber auch Natrium- und Kalzium-Kanäle, und blockiert nichtkompetitiv a- und ß-Adrenorezeptoren. Es mindert die Herzfrequenz, verzögert die sinuatriale und atrioventrikuläre Überleitung und verlängert das QT-Intervall. Negative Inotropie und vasodilatatorische Effekte an peripheren und koronaren Arterien senken den Blutdruck und den myokardialen Sauerstoffverbrauch, ohne dass das Herzzeitvolumen sinkt.4-6

KLINISCHE WIRKSAMKEIT: Das klinische Untersuchungsprogramm von Dronedaron umfasst sechs randomisierte doppelblinde Studien. In der Dosisfindungsstudie DAFNE* bei persistierendem Vorhofflimmern lässt sich keine Dosis-Wirkungs-Beziehung erkennen. Von den geprüften Tagesdosierungen (800 mg, 1.200 mg, 1.600 mg) ist nur die 800-mg-Dosis effektiv.7 In der ERATO*-Studie senken täglich 800 mg Dronedaron die Ventrikelfrequenz bei persistierendem Vorhofflimmern gegenüber Plazebo in Ruhe um 12, unter Belastung um 25 Schläge pro Minute.8
| * | DAFNE = Dronedarone Atrial FibrillatioN Study after Electrical Car-dio-ver-sion, ERATO = Efficacy and safety of dRonedArone for The cOntrol of ven-tri--cular rate during atrial fibrillation |
Die identisch konzipierten und gemeinsam publizierten multinationalen Studien EURIDIS** und ADONIS** untersuchen bei zusammen 1.237 Patienten mit nichtpermanentem Vorhofflimmern die Stabilisierung des Sinusrhythmus durch Dronedaron nach Kardioversion oder spontaner Konversion. 41% der Patienten haben strukturelle Herzkrankheiten, 16% Klappenerkrankungen, 57% eine Hypertonie und 17% eine Herzinsuffizienz NYHA I bis II. Herzinsuffizienz NYHA III und IV, Bradykardien, höhergradiger AV- oder SA-Block, frühere Torsade de pointes, Therapie mit Klasse I- oder III-Antiarrhythmika sowie relevante Organfunktionsstörungen sind Ausschlussgrund. 87% der Patienten hatten in den drei Monaten zuvor Symptome durch das Vorhofflimmern. Mehrheitlich sind sie mit Antiarrhythmika verschiedener Klassen vorbehandelt, 30% mit Amiodaron.9
| ** | EURIDIS = EURopean Trial In Atrial Fibrillation or Flutter Patients Receiving Dro-ne-da-rone for the MaIn-tenance of Sinus Rhythm ADONIS = American-Australian-African Trial with DronedarONe In Atrial Fibrillation or Flutter Patients for the Main-tenance of Sinus Rhythm |
Innerhalb von zwölf Monaten kommt es unter Plazebo bei 75,2%, unter Dronedaron bei 64,1% erneut zu Vorhofflimmern (Hazard Ratio [HR] 0,75; 95% Konfidenzintervall [CI] 0,65-0,87), das bei 46,0% bzw. 37,7% der Studienteilnehmer symptomatisch ist (HR 0,71; 95% CI 0,60-0,86). Die mittlere Herzfrequenz bei Rezidiv beträgt unter Plazebo 117 und unter Dronedaron 103 (p < 0,001). Krankenhausaufnahmen oder Todesfälle werden nach post-hoc Analysen von 30,9% auf 22,8% reduziert, die Mortalität allein unterscheidet sich jedoch nicht (Dronedaron 1% versus 0,7% unter Plazebo). Subgruppenanalysen ergeben keine auffälligen Befunde.9
Die ANDROMEDA***-Studie10 prüft nicht den Effekt von Dronedaron bei Vorhofflimmern, sondern auf den Krankheitsverlauf bei Patienten, die wegen sich verschlechternder Herzinsuffizienz stationär aufgenommen werden und bei denen im Vormonat mindestens einmal Dyspnoe bei geringer Belastung oder in Ruhe (NYHA III oder IV) aufgetreten ist. In der Vorgeschichte ist bei 40% eine mäßige (NYHA II) und bei 57% eine schwere Herzinsuffizienz (NYHA III) bekannt. Vorhofflimmern oder -flattern findet sich in der Anamnese bzw. bei Randomisierung nur bei 38% bzw. 25% der Patienten. Die - erst 2008 vollständig publizierte - Studie wurde 2003 nach Aufnahme von 627 der geplant 1.000 Patienten und einer medianen Laufzeit von nur zwei Monaten abgebrochen, weil unter Dronedaron signifikant mehr Todesfälle auftraten als unter Plazebo (8,1% vs. 3,8%; HR 2,13; 95% CI 1,07-4,25). Vor allem kardiovaskuläre Todesfälle nehmen zu, insbesondere infolge fortschreitender Herzinsuffizienz. Subgruppenanalysen weisen eine deutlich eingeschränkte linksventrikuläre Funktion und eine auch nur mäßig eingeschränkte Nierenfunktion als Risikofaktoren aus.10
| *** | ANDROMEDA = ANti-arrhythmic Trial with DROnedarone in Mo-de--rate to Severe CHF Evaluating Morbidity DecreAse |
Den Arzneimittelbehörden FDA und EMA reichten die Ergebnisse dieser Studien auch für eine Zulassung mit Auflagen nicht aus, sodass die Anträge aus dem Jahr 2005 zurückgezogen werden mussten.6 Gefordert wurden eine aktiv kontrollierte Studie sowie weitere Daten zum Einfluss von Dronedaron auf Morbidität und Mortalität.5
Die daraufhin initiierte DIONYSOS****-Studie vergleicht täglich 800 mg Dronedaron mit 200 mg Amiodaron (nach Aufsättigung mit 600 mg/d für 28 Tage) bei 504 Patienten, die seit mindestens 72 Stunden an Vorhofflimmern leiden und bei denen nach Meinung der Behandelnden der Sinusrhythmus nach Kardioversion erhalten werden sollte. Ergebnisse liegen bisher nur FDA und EMA vor.5,11 Der kombinierte Endpunkt aus Rezidiv des Vorhofflimmerns oder Studienabbruch wegen fehlender Wirkung oder schlechter Verträglichkeit tritt unter Dronedaron in zwölf Monaten signifikant häufiger auf als unter Amiodaron (75% vs. 59%; HR 1,59; 95% CI 1,28-1,98). Unter Dronedaron sind vor allem Rezidive des Vorhofflimmerns häufiger (66% vs. 42%); wie oft sie symptomatisch sind, bleibt unklar. Beim Hauptsicherheitsendpunkt, der Störwirkungen an Schilddrüse, Lunge, Leber, Haut, Augen und Nervensystem erfasst, finden sich keine signifikanten Unterschiede (39,3% vs. 44,5%; HR 0,80; 95% CI 0,6-1,07).11 Die Ergebnisse belegen eine deutlich geringere antiarrhythmische Wirkung von Dronedaron, erlauben aber letztlich keine abschließende vergleichende Bewertung des klinischen Nutzens.
| **** | DIONYSOS = Efficacy and Safety of Dro-ne-darone ver-sus Amio-da-rone for the Maintenance of Sinus Rhythm in Pa-tients with Atrial Fibrillation |
Die ebenfalls 2005 begonnene ATHENA*****-Studie12 schließt 4.628 Patienten mit nichtpermanentem Vorhofflimmern ein, die mindestens einen weiteren ungünstigen Prognosefaktor aufweisen wie Alter über 70 Jahre, behandelter Bluthochdruck oder Diabetes. Patienten mit schwerer Herzinsuffizienz (NYHA IV), mit dekompensierter Herzinsuffizienz in den vier Wochen vor Studienbeginn, akutem Infarkt, Bradykardie oder Überleitungsstörungen sind ausgeschlossen. Zu Studienbeginn liegt entweder ein Sinusrhythmus vor oder es ist - bei aktuellem Vorhofflimmern oder -flattern (25%) - eine Kardioversion vorgesehen. 86% haben einen Bluthochdruck, 30% eine koronare Herzkrankheit und 16% eine Klappenkrankheit. Bei 17% bzw. 4% ist eine Herzinsuffizienz NYHA II bzw. III bekannt.12
| ***** | ATHENA = A Placebo-Controlled, Double-Blind, Parallel Arm Trial to Assess the Efficacy of Dronedarone for the Pre-ven-tion of Car-dio-vas-cular Hospi-ta-li-zation or Death from Any Cause in PatiENts with Atrial Fib-rilla-tion/Atrial Flutter |
Gegenüber Plazebo vermindert Dronedaron nach im Mittel 21 Monaten den kombinierten primären Endpunkt Tod oder erste stationäre Aufnahme wegen kardiovaskulärer Ereignisse von 39,4% auf 31,9% (HR 0,76; 95% CI 0,69-0,84). Das Ergebnis ist über eine Reihe von Subgruppen nahezu gleich. Insbesondere schneiden Patienten mit struktureller Herzkrankheit, bekannter Herzinsuffizienz oder reduzierter Ejektionsfraktion nicht schlechter ab. Der Nutzen beschränkt sich auf die Minderung stationärer Aufnahmen wegen kardiovaskulärer Ereignisse (36,9% vs. 29,3%; p < 0,001), vor allem solcher wegen Vorhofflimmerns (21,9% vs. 14,6%). Die Mortalität bleibt unbeeinflusst (2,5% vs. 2,6%).12
Warum die Patienten wegen Vorhofflimmerns stationär aufgenommen werden, bleibt allerdings unklar,13 da die Gründe weder systematisch erfasst noch durch ein unabhängiges und verblindetes Komitee evaluiert werden.5,14 Von der EMA geforderte post-hoc erhobene Daten weisen darauf hin, dass die Aufnahmen vor allem mit Behandlungen des Vorhofflimmerns im Zusammenhang stehen. Die Reduktion stationärer Aufnahmen wegen kardiovaskulärer Ereignisse um absolut 7,5% ist damit vor allem durch die antiarrhythmische Wirkung von Dronedaron zu erklären.5 In der Werbung führt das zur Behauptung, dass es als erstes Antiarrhythmikum "nachweislich die kardiovaskuläre Prognose verbessert."15
VERTRÄGLICHKEIT: Im Plazebovergleich9,12 sind unter Dronedaron signifikant häufiger Bradykardien (2,7% bis 3,5% vs. 1,2% bis 2,0%), QT-Verlängerungen (1,7% vs. 0,6%), Magen-Darm-Beschwerden (26% vs. 22%) wie Übelkeit (5,3% vs. 3,1%) und Durchfall (7,1% bis 9,7% vs. 4,9% bis 6,2%) sowie Hautreaktionen (10,3% vs. 7,6%) beschrieben. Hyperthyreosen kommen seltener (8,4% vs. 14,1%), Hypothyreosen (5,5% vs. 3,5%) und Studienabbrüche wegen Störwirkungen (12,7% vs. 8,1%) häufiger vor als unter Plazebo. Reversible Anstiege des Serumkreatinins, meist in der ersten Woche, treten ebenfalls gehäuft auf (2,4% bis 4,7% vs. 1,0% bis 1,3%). Sie werden auf eine Hemmung der tubulären Sekretion von Kreatinin zurückgeführt und sollen kein Zeichen einer Nierenfunktionseinschränkung sein.16 Lungen- und Leberfunktionsstörungen, Neuropathien und Hornhauteinlagerungen sind bisher nicht gehäuft berichtet worden,4,5 treten jedoch auch unter Amiodaron erst bei längerer Einnahme auf.
Im Vergleich zu Amiodaron scheinen Schilddrüsenfunktionsstörungen (0,8% vs. 5,9%) und neurologische Symptome (1,2% vs. 6,7%) sowie Abbrüche der Medikation (5,2% vs. 11,0%) unter Dronedaron seltener, Magen-Darm-Beschwerden dagegen häufiger (12,9% vs. 5,1%) zu sein.5,11 Eine abschließende Bewertung ist wegen unzureichender Langzeitdaten nicht möglich.13
Bei Patienten mit instabiler Herzinsuffizienz NYHA III oder IV erhöht Dronedaron die Sterblichkeit und ist deshalb kontraindiziert.4,10 Bei nicht länger als drei Monate bekannter stabiler Herzinsuffizienz NYHA III und bei Ejektionsfraktion unter 35% wird von der Anwendung mangels Erfahrung abgeraten.4,12 Eine ausreichende Trennschärfe zu Patienten mit NYHA II scheint im Einzelfall zweifelhaft.13
WECHSELWIRKUNGEN: Für Dronedaron sind vielfältige Interaktionen möglich, sodass bei jeder Begleitmedikation eine Überprüfung erfolgen sollte (siehe Eigenschaften, S. 17).
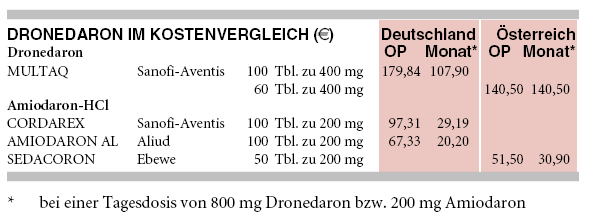
KOSTEN: Die Kosten für eine Therapie mit täglich zweimal 400 mg Dronedaron liegen pro Monat bei 108 €. Damit ist es mehr als fünfmal teurer als Amiodaron, das generisch (z.B. AMIODARON AL) in einer für die Dauertherapie üblichen Tagesdosis von 200 mg für 20 € pro Monat erhältlich ist. Das britische NICE****** lehnt in einer ersten Stellungnahme eine Kostenübernahme ab, da eine Kosteneffektivität im Vergleich zu anderen Antiarrhythmika nicht gesehen wird.17
| ****** | NICE = National Institute for Health and Clinical Excellence |
Das Antiarrhythmikum Dronedaron (MULTAQ) - ein Analog von Amiodaron (CORDAREX, Generika) ohne Jod-Substituenten - ist zur Rhythmus- und Frequenzkontrolle bei nichtpermanentem Vorhofflimmern zugelassen.
Gegenüber Plazebo senkt Dronedaron die Rezidivrate eines Vorhofflimmerns. Auch Krankenhausaufnahmen wegen Vorhofflimmerns werden gegenüber Scheinmedikament gemindert. Sterblichkeit und andere kardiovaskuläre Ereignisse bleiben unbeeinflusst.
Im Vergleich zu Amiodaron verhindert Dronedaron Rezidive eines Vorhofflimmerns deutlich schlechter.
Bevorzugte Strategie bei Vorhofflimmern ist die Kontrolle der Ventrikelfrequenz. Dronedaron ist hier zwar Plazebo überlegen, ein Vergleich mit Standardmitteln wie Betablockern fehlt jedoch.
Unter den Störwirkungen dominieren Übelkeit, Durchfall und Hautreaktionen. Häufig sind zudem Bradykardie, QT-Verlängerung und - klinisch wahrscheinlich nicht relevanter - Kreatininanstieg. Gegenüber Amiodaron treten relevante Störwirkungen insgesamt gleich häufig, Schilddrüsenfunktionsstörungen und neurologische Symptome seltener und Magen-Darm-Beschwerden häufiger auf.
Zahlreiche relevante Interaktionen sind zu beachten.
Bei Patienten mit instabiler Herzinsuffizienz NYHA III-IV verschlechtert Dronedaron die Symptomatik, erhöht die Mortalität und ist kontraindiziert.
Bei derzeitiger Datenlage sehen wir keine Indikation für die teure Amiodaronvariante.
| (R = randomisierte Studie, M = Metaanalyse) | ||
| 1 | LAFUENTE-LAFUENTE, C. et al.: BMJ 2010; 340: 40-45 | |
| 2 | FUSTER, V. et al.: J. Am. Coll. Cardiol. 2006; 48: 854-906 | |
| M | 3 | DOYLE, J.F. et al.: Mayo Clin. Proc. 2009; 84: 234-42 |
| 4 | Sanofi-Aventis: Fachinformation MULTAQ, Stand Dez. 2009 | |
| 5 | EMA: Europ. Beurteilungsbericht (EPAR) MULTAQ, Stand Dez. 2009 http://www.ema.europa.eu/humandocs/Humans/EPAR/multaq/multaq.htm | |
| 6 | SCHAFER, J.A. et al.: Cardiovasc. Ther. 2010; 28: 38-47 | |
| R | 7 | TOUBOUL, P. et al.: Eur. Heart J. 2003; 24: 1481-7 |
| R | 8 | DAVY, J.M. et al.: Am. Heart J. 2008; 156: e1-9 |
| R | 9 | SINGH, B.N. et al.: N. Engl. J. Med. 2007; 357: 987-99 |
| R | 10 | KØBER, L. et al.: N. Engl. J. Med. 2008; 358: 2678-87 |
| 11 | Sanofi-Aventis: MULTAQ (Dronedarone) Briefing Document: www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/ Drugs/CardiovascularandRenalDrugsAdvisoryCommittee/UCM134981.pdf | |
| R | 12 | HOHNLOSER, S.H. et al.: N. Engl. J. Med. 2009; 360: 668-78 |
| 13 | KARKOWSKY, A. (FDA): Diavortrag Advisory Committee Meeting 18. März 2009; http://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeeting Materials/Drugs/CardiovascularandRenalDrugsAdvisoryCommittee/UCM136998.pdf | |
| 14 | HOHNLOSER, S.H. et al.: J. Cardiovasc. Electrophysiol. 2008; 19: 69-73 | |
| 15 | Sanofi-Aventis: Rundschreiben vom Jan. 2010 | |
| R | 16 | TSCHUPPERT, Y. et al.: Br. J. Clin. Pharmacol. 2007; 64: 785-91 |
| 17 | NICE: Atrial fibrillation-dronedarone: appraisal consultation document: http://www.nice.org.uk/guidance/index.jsp?action=article&o=46768 |
© 2010 arznei-telegramm, publiziert am 12. Februar 2010
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
