VERHÜTUNGSPILLE ZOELY
Seit Anfang 2012 ist mit ZOELY ein zweites kombiniertes orales Kontrazeptivum auf dem Markt, bei dem auf das jahrzehntelang übliche synthetische Östrogen Ethinylestradiol (EE) verzichtet wird. Die monophasische Pille enthält stattdessen das körpereigene Estradiol sowie Nomegestrol, ein international wenig gebräuchliches Gestagen. Eine Estradiol-Nomegestrolazetat-Kombination wird bislang lediglich in Frankreich und nur gegen Wechseljahresbeschwerden angeboten.1 2009 wurde mit QLAIRA das erste EE-freie kombinierte Kontrazeptivum eingeführt, das aus Estradiolvalerat, der veresterten Form von Estradiol, und dem international ebenfalls wenig bekannten Gestagen Dienogest besteht und dessen kompliziertes Vierphasenschema Anwendungsfehler begünstigt (a-t 2009; 40: 62-3).
In den USA ist ein Antrag auf Zulassung von ZOELY im November 2011 zum zweiten Mal gescheitert. Es wird vermutet, dass die US-amerikanische Zulassungsbehörde wegen der zunehmenden Sicherheitsbedenken gegenüber neueren kombinierten hormonellen Kontrazeptiva, beispielsweise Drospirenon-haltigen Pillen oder dem Verhütungspflaster EVRA (EE + Norelgestromin;
a-t 2012; 43: 15-6, a-t 2011; 42: 109), künftig vor der Zulassung Langzeitdaten insbesondere zum Risiko venöser Thromboembolien fordert.1,2
EIGENSCHAFTEN: Nomegestrolazetat ist ein Progesteronabkömmling, der selektiv an Progesteronrezeptoren bindet und antigonadotrope und antiöstrogene Effekte hat. Die kontrazeptive Wirksamkeit beruht im Wesentlichen auf einer Hemmung der Ovulation. Das enthaltene Estradiol ist mit dem körpereigenen 17β-Estradiol identisch. Es trägt zwar ebenfalls zur empfängnisverhütenden Wirksamkeit bei, soll aber vor allem die durch Nomegestrolazetat unterdrückte endogene Östrogenproduktion ausgleichen und die Gebärmutterschleimhaut stabilisieren, um einen regelmäßigen Zyklus zu erzielen.1
WIRKSAMKEIT: In zwei offenen Studien aus Europa bzw. den USA, von denen nur die europäische vollständig publiziert ist,3 nehmen mehr als 4.000 Frauen zwischen 18 und 50 Jahren 3 : 1 randomisiert ein Jahr lang die Estradiol-Nomegestrolazetat-Kombination oder 30 µg EE plus 3 mg Drospirenon (YASMIN u.a.) ein. Die Rate der Studienabbrecherinnen ist mit etwa 25% in der europäischen und 40% in der US-amerikanischen Untersuchung auffällig hoch und unter ZOELY dabei jeweils numerisch höher als unter dem Drospirenon-haltigen Kontrazeptivum.1 Primärer Endpunkt ist die Rate der Schwangerschaften pro 100 Frauenjahre (Pearl Index) in der prädefinierten Subgruppe der 18- bis 35-jährigen Frauen. Ausgewertet werden nur Zyklen, in denen das Risiko einer Schwangerschaft bestand. In der europäischen Studie beträgt der Pearl Index 0,38 (95% Konfidenzintervall [CI] 0,10-0,97; 4 von 1.315 Frauen werden schwanger) und liegt damit im Bereich anderer kombinierter oraler Kontrazeptiva einschließlich der Drospirenon-haltigen Vergleichspille (Pearl Index 0,81; 95% CI 0,17-2,35; 3/442).1,3 In der US-amerikanischen Studie schneiden beide Pillen schlechter ab (Pearl Index unter Estradiol plus Nomegestrolazetat 1,16, unter EE plus Drospirenon 1,89).1 Die Ursache bleibt unklar. Ähnliche Unterschiede sind aber auch beim intravaginalen Ring NUVARING aufgefallen (EE + Etonogestrel; Pearl Index 0,65 in Europa gegenüber 1,75 in USA; vgl. a-t 2003; 34: 17-8).
STÖRWIRKUNGEN: Die europäische Arzneimittelbehörde EMA bezeichnet das Sicherheitsprofil der Neuerung als "schlechter" als das des Drospirenon-haltigen Vergleichskontrazeptivums.1 Mehr Frauen klagen über unerwünschte Effekte (75,3% versus 69,0%) oder brechen die Einnahme deswegen vorzeitig ab (17,1% vs. 10,1%). Häufiger sind vor allem Akne, Gewichtszunahme, Blutungsunregelmäßigkeiten (unter ZOELY jeweils über 10%) und psychiatrische Störwirkungen (z.B. verminderte Libido oder Stimmungsschwankungen, ohne Häufigkeitsangabe).1
Zwischenblutungen betreffen unter ZOELY 15% bis 20% der Anwenderinnen. Das Ausbleiben einer Abbruchblutung liegt in den Zyklen 1 bis 12 in einem Bereich von 18% bis 32%.4 Die Rate anhaltender Amenorrhoen nimmt im Studienverlauf zu: So haben z.B. 2% der Frauen ab dem 1. Zyklus bis zum Studienende keine Abbruchblutung, ab dem 9. Zyklus sind es 9%.1 Wenn zwei Abbruchblutungen hintereinander ausbleiben, muss vor der weiteren Einnahme eine Schwangerschaft ausgeschlossen werden.4
Nach Einschätzung der EMA ist die hohe Amenorrhoerate ein Hinweis darauf, dass die östrogene Stimulation des Endometriums unter ZOELY geringer ist als unter anderen kombinierten oralen Kontrazeptiva. Die Estradioldosis wurde ausschließlich deshalb gewählt, weil sie in Kombination mit Nomegestrolazetat in einem französischen Präparat gegen Wechseljahresbeschwerden verwendet wird. Dosisfindungsstudien bei prämenopausalen Frauen wurden für die Estradiolkomponente von ZOELY nicht durchgeführt. Ob der Gehalt aber bei diesen die antiöstrogenen Effekte von Nomegestrolazetat ausgleicht, bleibt angesichts der starken Suppression der endogenen Produktion offen.1 Bedenken bestehen insbesondere bei Jugendlichen unter 18 Jahren, da viele physiologische Prozesse wie der Aufbau der Knochen und der Sexualorgane von einem ausreichenden Östrogenangebot abhängen.1 In dieser Altersgruppe sind Wirksamkeit und Unbedenklichkeit gar nicht geprüft.1,4 Bei 14- bis 17-Jährigen liegen die Estradiolspiegel nach einmaliger Einnahme zudem um 36% unter denen erwachsener Anwenderinnen. Dennoch ist die Zulassung nicht ausdrücklich auf Frauen ab 18 Jahren begrenzt. Die europäische Behörde ist der Meinung, es reiche aus, in der Fachinformation (auf den hinteren Seiten, -Red.) auf das Fehlen klinischer Daten und die Pharmakokinetik bei Jugendlichen hinzuweisen.1
Von "natürlichen" Östrogenen erhofft man sich eine gegenüber dem synthetischen EE geringere Thrombogenität. Ob dies zutrifft, muss jedoch durch klinische Studien belegt werden. Entsprechende Daten gibt es bislang weder für ZOELY noch für das Estradiolvalerat-haltige QLAIRA.
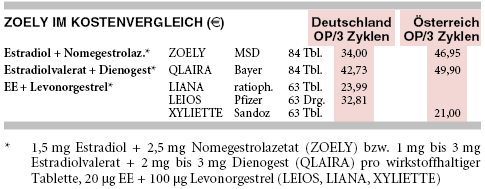
KOSTEN: Die dreimonatige Verhütung mit ZOELY (1,5 mg Estradiol plus 2,5 mg Nomegestrolazetat/Tablette) kostet 34 € und damit 40% mehr als mit einer preisgünstigen niedrigdosierten Levonorgestrel-Kombination (20 µg EE plus 100 µg Levonorgestrel; LIANA: 24 €). Für die Estradiolvalerat-Dienogest-Kombination QLAIRA (1 mg bis 3 mg Estradiolvalerat plus 2 mg bis 3 mg Dienogest; 43 €) ist gegenüber ZOELY 25% mehr aufzuwenden.
Mit ZOELY wird ein weiteres kombiniertes Kontrazeptivum ohne das synthetische Östrogen Ethinylestradiol angeboten. Die Neuerung enthält stattdessen Estradiol sowie das international wenig gebräuchliche Nomegestrol.
Schwangerschaften verhütet die neue Pille ebenso gut wie ein Drospirenon-haltiges Kontrazeptivum (YASMIN u.a.). Sie wird aber schlechter vertragen, insbesondere Akne, Blutungsunregelmäßigkeiten, Gewichtszunahme und psychiatrische Störwirkungen kommen vermehrt vor.
Das Thromboembolierisiko ist unbekannt.
Ob die Estradioldosis der Kombination ausreicht, um die antiöstrogenen Effekte des enthaltenen Gestagens auszugleichen, ist unklar. Bedenken bestehen hier insbesondere bei Jugendlichen unter 18 Jahren, für die Daten zu Wirksamkeit und Unbedenklichkeit fehlen.
Beim derzeitigen Kenntnisstand raten wir von ZOELY ab. Für die Verhütung stehen genügend besser erprobte und verträglichere Alternativen zur Verfügung.
| (R =randomisierte Studie) | |
| 1 | EMA: Europ. Beurteilungsbericht (EPAR) ZOELY, Stand Okt. 2011 http://www.emea.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/001213/WC500115833.pdf |
| 2 | Scrip 2011; Nr. 3574: 1, 5 |
| R 3 | MANSOUR, D. et al.: Eur. J. Contracept. Reprod. Health Care 2011; 16: 430-43 |
| 4 | MSD: Fachinformation ZOELY, Stand Nov. 2011 |
© 2012 arznei-telegramm, publiziert am 9. März 2012
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
