KNOCHENMETASTASEN / MULTIPLES MYELOM
... Prophylaxe von Skelettkomplikationen
Bei etwa 70% der Patienten, die an Brust- oder Prostatakrebs sterben, finden sich autoptisch Knochenmetastasen, bei Lungen-, Schilddrüsen- und Nierenkrebs sind es etwa 30% bis 40%.1 Bei Multiplem Myelom sind Osteolysen häufig bereits bei Diagnose vorhanden.2 Knochenmetastasen und Osteolysen führen häufig zu Schmerzen, Hyperkalziämie und skelettbezogenen Komplikationen, zu denen pathologische Frakturen und Rückenmarkskompression sowie notwendig werdende Strahlentherapie oder Operation des Knochens gerechnet werden.
Seit Längerem stehen zur Prävention dieser Komplikationen Bisphosphonate zur Verfügung, seit August 2011 auch der gegen das Tumornekrose-Zytokin RANKL* gerichtete monoklonale Antikörper Denosumab (XGEVA). Die unterschiedlich weit gefassten zugelassenen Anwendungsgebiete sind nicht alle gleich gut durch die Evidenz begründet: So darf Clodronat (BONEFOS u.a.)3 bei allen Osteolysen infolge von Knochenmetastasen solider Tumoren oder infolge hämatologischer Neoplasien wie Multiplem Myelom eingenommen werden. Zoledronat (ZOMETA) darf hingegen auch ohne Osteolyse bei allen fortgeschrittenen, auf das Skelett ausgedehnten Tumorerkrankungen4 verwendet werden, Denosumab5 nur bei Knochenmetastasen solider Tumoren und damit nicht bei Multiplem Myelom. Ibandronat (BONDRONAT, Generika)6 ist bei Knochenmetastasen eines Mammakarzinoms zugelassen, Pamidronat (AREDIA, Generika)7 wiederum nur bei Osteolysen eines vorbehandelten Mammakarzinoms oder eines gleichzeitig chemotherapeutisch behandelten Multiplen Myeloms im Stadium III (Stadieneinteilung siehe Kasten).
| * | RANKL = Receptor Activator of Nuclear Factor Kappa B Ligand |
Eine Verlängerung des Lebens ist bei Knochenmetastasen solider Tumoren bislang für keines der Mittel hinreichend belegt, bei Multiplem Myelom weist eine Studie auf einen möglichen Überlebensvorteil durch Zoledronat hin.
BRUSTKREBS: Der Nutzen von Pamidronat in der zugelassenen Dosierung von 90 mg intravenös (i.v.) wird in zwei plazebokontrollierten Studien untersucht.8,9 In einer Studie mit 382 Frauen unter Chemotherapie, die mindestens eine osteolytische Metastase aufweisen, senkt Pamidronat (alle vier Wochen) den Anteil der Frauen mit mindestens einer skelettbezogenen Komplikation** gegenüber Plazebo innerhalb von zwölf Monaten von 56% auf 43% (p = 0,008). Die Zeit bis zur ersten skelettbezogenen Komplikation wird im Median von 7 auf 13 Monate verlängert (p = 0,005). Pathologische nichtvertebrale Frakturen (20% vs. 30%), Strahlentherapie und Operation des Knochens (19% vs. 33% bzw. 4% vs. 10%) sind unter dem Bisphosphonat signifikant seltener.8 Unter hormoneller Therapie hingegen verringert Pamidronat in einer zweiten Studie9 mit 372 Frauen die Komplikationsrate innerhalb von zwölf Monaten nur numerisch (47% vs. 55%; p = 0,109). Die Zeit bis zur ersten Komplikation wird nicht signifikant verlängert (im Median von 7 auf 11 Monate; p = 0,163). Auch am Ende der eigentlich nur zur Beurteilung der Sicherheit geplanten plazebokontrollierten Extensionsstudie über weitere 12 Monate findet sich kein signifikanter Effekt. Die US-amerikanische Arzneimittelbehörde FDA sieht die Wirksamkeit zwar auch für Frauen unter Hormontherapie als belegt an.10 Anders als hierzulande weist die dortige Fachinformation jedoch darauf hin, dass der Effekt geringer zu sein scheint als bei Frauen unter Chemotherapie.11 Dem FDA-Reviewer zufolge stellte sich die Frage, ob der geringe Effekt die Unannehmlichkeiten der monatlichen Infusion wert sei.10
| ** | In den betrachteten randomisierten Studien dieser Übersicht werden zum Teil auch mehrere Ereignisse eines Patienten im primären Studienendpunkt erfasst. Demgegenüber stellen die Zeit bis zur ersten skelettbezogenen Komplikation und der Anteil an Patienten mit mindestens einer skelettbezogenen Komplikation (im Folgenden verkürzt als Komplikationsrate bezeichnet) konservative Endpunkte dar.14 Die Wirksamkeit kann dennoch überschätzt werden, wenn in Studien auch radiologisch gescreente Brüche zu den pathologischen Frakturen gezählt werden, da deren klinische Relevanz unklar ist. |
In beiden Studien nehmen Schmerzen unter dem Bisphosphonat geringer zu und der Analgetikaverbrauch steigt weniger an. Ob die Unterschiede (im Mittel 0,7 bis 1,3 Punkte auf einer 9 Punkte umfassenden Skala) auch immer klinisch relevant sind, bleibt offen. Die Lebensqualität verschlechtert sich in der Studie mit Chemotherapie in einem von zwei Scores signifikant weniger.10
Zoledronat wird in einer dreiarmigen Studie12 in zwei Dosierungen - 4 mg und 8 mg (später wegen Nephrotoxizität in diesem Arm ebenfalls 4 mg) i.v. 12 Monate lang alle drei bis vier Wochen - mit Pamidronat (90 mg i.v. alle drei bis vier Wochen) verglichen. Die Studienteilnehmer sind 1.130 Patienten mit Brustkrebs (zu 99,4% Frauen)13 sowie 513 Patienten mit Multiplem Myelom im Stadium III. In der zugelassenen Dosierung von 4 mg wirkt Zoledronat bei gemeinsamer Auswertung beider Indikationen ähnlich wie Pamidronat (Komplikationsrate 44% vs. 46%; 95% CI der Differenz -7,9% bis 3,7%). Einer Subgruppenanalyse zufolge finden sich weder bei Brustkrebs mit Chemo- bzw. Hormontherapie noch bei Multiplem Myelom Wirksamkeitsunterschiede.14
Schmerz- und Analgetikascores unterscheiden sich ebenfalls nicht. Die Daten zur Lebensqualität sind inkonsistent: Sie wird nur in einem von zwei Scores sowohl unter Pamidronat als auch in der Gruppe, die zunächst 8 mg Zoledronat erhält, signifikant besser bewertet als in der 4-mg-Zoledronat-Gruppe.14
An der Studie nahmen auch Brustkrebspatienten mit ausschließlich nichtosteolytischen Knochenmetastasen teil. Bei diesen weist eine Subgruppenanalyse nicht auf bessere Wirksamkeit von Zoledronat hin.14 Da die Wirksamkeit von Pamidronat jedoch nur bei vorhandener Osteolyse belegt ist, erscheint uns der Nutzen von Zoledronat bei ausschließlich nichtosteolytischen Metastasen fraglich. Insgesamt sehen wir keinen Wirkvorteil von Zoledronat gegenüber Pamidronat.
Für Ibandronat ist eine Reduktion des Risikos skelettbezogener Komplikationen weniger zuverlässig belegt. In einer gemeinsamen Auswertung von zwei dreiarmigen Studien mit 846 Frauen,15 die täglich für bis zu 96 Wochen 20 mg bzw. 50 mg Ibandronat oder Plazebo einnehmen, wird für die zugelassene 50-mg-Dosierung gegenüber Plazebo kein signifikanter Einfluss auf die Zeit bis zur ersten Komplikation errechnet (im Median 90 Wochen vs. 65 Wochen; p = 0,089).16 Sowohl unter 20 mg als auch unter 50 mg Ibandronat sterben mehr Patientinnen als unter Plazebo (17% bzw. 20% vs. 15%).15 In einer ebenfalls dreiarmigen Studie mit 2 mg oder 6 mg Ibandronat i.v. oder Plazebo i.v. alle drei bis vier Wochen für bis zu zwei Jahre, an der 466 Frauen teilnehmen, verzögert das Bisphosphonat in der zugelassenen Dosierung von 6 mg i.v. das Auftreten der ersten Komplikation zwar von im Median 33 Wochen unter Plazebo auf 51 Wochen (p = 0,018). Bei der Komplikationsrate wird Signifikanz jedoch knapp verfehlt (51% vs. 62%; p = 0,052).17
Zu Clodronat per os liegen bei Brustkrebs mit Knochenmetastasen nur kleine methodisch mangelhafte Studien ohne konsistente Effekte auf die Raten von Frakturen und Strahlentherapien des Knochens vor.18-21 Ibandronat und Clodronat sind in den USA zur Prophylaxe bei Knochenmetastasen nicht zugelassen.
Der Antikörper Denosumab mindert in einer Dosierung von 120 mg subkutan gegenüber Zoledronat 4 mg i.v.*** jeweils alle vier Wochen in einer Studie22 mit 2.046 Patienten (99% Frauen) die Komplikationsrate von 37% auf 31% nach medianer Nachbeobachtung von 17 Monaten (Hazard Ratio [HR] 0,82; 95% Konfidenzintervall [CI] 0,71-0,95). Dabei beeinflusst Denosumab vor allem die Endpunktkomponenten Bestrahlung des Knochens (8% vs. 11,7%) und pathologische Frakturen (20,7% vs. 23,3%) stärker.23 Konsistente signifikante Unterschiede in Bezug auf Schmerzparameter, Lebensqualität und Analgetikagebrauch finden sich nicht.24,25
| *** | Bei Niereninsuffizienz wurde die Dosierung gemäß Fachinformation reduziert bzw. die Therapie pausiert. |
Vorteile bietet die Applikationsform: Die subkutane Injektion des Antikörpers ist einfacher durchzuführen als die Infusion von Zoledronat über mindestens 15 Minuten oder von Pamidronat über zwei Stunden. Anders als Pamidronat und Zoledronat darf Denosumab zudem auch bei schwerer Niereninsuffizienz oder Dialyse uneingeschränkt angewendet werden. Hierzu liegen anscheinend aber lediglich Ergebnisse aus einer Pharmakokinetik-Studie vor.24
Die aktuelle Leitlinie der American Society of Clinical Oncology (ASCO) sieht Wirkunterschiede zwischen Pamidronat, Zoledronat und Denosumab bei Brustkrebs als nicht hinreichend belegt an. Die optimale Therapiedauer ist nicht bekannt.26
PROSTATAKREBS: Bei fortgeschrittenem Prostatakrebs ist eine Minderung skelettbezogener Komplikationen unter Bisphosphonaten nur für Zoledronat belegt.27 Bei Knochenmetastasen eines hormonrefraktären Prostatakarzinoms verringern 4 mg Zoledronat i.v. alle drei Wochen in einer Studie mit 643 Männern die Komplikationsrate gegenüber Plazebo innerhalb von 15 Monaten von 44% auf 33% (95% CI der Differenz -20% bis -2%).28 Die Zeit bis zur ersten Komplikation wird signifikant verlängert (HR 0,67; 95% CI 0,49-0,91).29 Als skelettbezogene Komplikation wird in dieser Studie auch die Änderung der antineoplastischen Therapie zur Behandlung von Knochenschmerzen gewertet. Ausschluss dieser Ereignisse ändert das Ergebnis aber nicht. In einem weiteren Studienarm, in dem - wie in der Studie bei Brustkrebs - zunächst 8 mg und später wegen Nephrotoxizität 4 mg angewendet werden, sinkt die Komplikationsrate nur numerisch von 44% auf 38% (p = 0,222) und die Zeit bis zur ersten Komplikation wird nicht signifikant verlängert.14 Diese Inkonsistenz, geringere Wirksamkeit trotz zunächst höherer Dosierung, erachten sowohl die Europäische Arzneimittelbehörde EMA als auch die FDA als problematisch.14,30 Laut Fachinformation sollen die Behandlungseffekte bei blastischen Läsionen weniger ausgeprägt sein.4
Schmerzen nehmen unter Zoledronat zwar zu einigen Zeitpunkten im Mittel statistisch signifikant geringer zu als unter Plazebo.4,31 Die klinische Relevanz ist jedoch unklar. Lebensqualität und Verbrauch von Analgetika unterscheiden sich nicht.14 Der Nutzen von Zoledronat erscheint somit weniger zuverlässig nachgewiesen als bei Brustkrebs.
120 mg Denosumab senken die Komplikationsrate gegenüber 4 mg Zoledronat i.v.*** jeweils alle vier Wochen in einer Studie32 mit 1.904 Männern mit hormonresistentem Prostatakrebs von 41% auf 36% nach medianer Nachbeobachtung von zwölf bzw. elf Monaten (HR 0,82; CI 0,71-0,95).24 Beeinflusst wird vor allem die Endpunktkomponente Bestrahlung des Knochens (18,6% vs. 21,3%).23 Konsistente signifikante Unterschiede bei Schmerz- und Lebensqualitätsparametern sowie Analgetikagebrauch finden sich nicht.24,25
In der aktuellen S3-Leitlinie zum Prostatakarzinom wird bei Knochenmetastasen im hormonrefraktären Stadium Zoledronat empfohlen. Die Wirksamkeit von Denosumab wird als mindestens gleichwertig eingestuft.33
ANDERE SOLIDE TUMOREN: Bei Patienten mit Knochenmetastasen eines Bronchialkarzinoms oder anderer solider Tumoren außer Brust- und Prostatakrebs senken 4 mg Zoledronat i.v. alle drei Wochen innerhalb von neun Monaten in einer Studie34 mit 773 Patienten die Komplikationsrate gegenüber Plazebo nicht signifikant von 44% auf 38% (p = 0,127). Die Zeit bis zur ersten skelettbezogenen Komplikation wird im Median von 5,4 Monaten auf 7,6 Monate verlängert (p = 0,026). Hinsichtlich Schmerz- und Analgetikascores sowie Lebensqualität unterscheiden sich die Gruppen nicht.14
Für Clodronat per os finden wir in vier randomisierten Studien keine ausreichenden Belege eines Nutzens hinsichtlich skelettbezogener Komplikationen.35-38
120 mg Denosumab alle vier Wochen sind in einer Studie39 mit 1.776 Patienten mit soliden Tumoren außer Brust- und Prostatakrebs oder mit multiplem Myelom gegenüber Zoledronat 4 mg i.v.*** in der Prävention skelettbezogener Komplikationen nicht unterlegen. Ein Wirkvorteil ist jedoch nicht hinreichend belegt (absolut 31,4% vs. 36,3%; HR 0,84; 95% CI 0,71-0,98; nicht signifikant überlegen nach Adjustierung für multiples Testen).24
| *** | Bei Niereninsuffizienz wurde die Dosierung gemäß Fachinformation reduziert bzw. die Therapie pausiert. |
Insgesamt erscheint uns der Nutzen von Bisphosphonaten und Denosumab hier fraglich.
MULTIPLES MYELOM: Bei symptomatischem Multiplem Myelom (siehe Kasten) ist der Nutzen von Bisphosphonaten gut dokumentiert. 90 mg Pamidronat i.v. alle vier Wochen senken in einer Studie mit 392 Patienten mit Multiplem Myelom im Stadium III, die wenigstens eine Osteolyse aufweisen und chemotherapeutisch behandelt werden, die Komplikationsrate gegenüber Plazebo nach neun Anwendungen von 41% auf 24% (p < 0,001). Gemindert werden pathologische Frakturen (17% vs. 30%; p = 0,004) und Strahlentherapie des Knochens (14% vs. 22%; p = 0,05).40 Nichtvertebrale Frakturen sollen hingegen nicht signifikant reduziert werden.41 Auch bei Schmerzen ist ein Vorteil gegenüber Plazebo nicht hinreichend belegt. Hinsichtlich Analgetikaverbrauch und Lebensqualität soll Pamidronat signifikant besser abschneiden. Genaue Angaben fehlen.40 Das Überleben wird nicht verlängert.41
Einnahme von täglich 1.600 mg Clodronat verringert in der MRC-MYELOMA****-VI-Studie mit 536 chemotherapeutisch behandelten Patienten gegenüber Plazebo den Anteil von Patienten mit nichtvertebralen Frakturen (6% vs. 11% nach medianer Nachbeobachtung von 2,8 Jahren; p = 0,036) sowie vertebralen Frakturen (38% vs. 55%; p = 0,01), nicht jedoch die Notwendigkeit einer Strahlentherapie. Hinreichende Belege für eine Minderung von Schmerzen und eine Steigerung der Lebensqualität fehlen. Das Überleben wird nicht verlängert.42 Zwei weitere methodisch mangelhafte Studien zu Clodronat43,44 eignen sich unseres Erachtens nicht zum Beleg eines Nutzens.
| **** | Myelomstudie des britischen Medical Research Council (MRC) |
Für Zoledronat ist im direkten Vergleich kein Vorteil gegenüber Pamidronat belegt. In einer Dosierung von 4 mg i.v. alle drei bis vier Wochen erweist es sich im oben bereits beschriebenen Vergleich mit Pamidronat, an dem auch Patienten mit Brustkrebs teilnehmen, als nicht unterlegen, aber auch nicht überlegen.12,14 Hinweise auf einen Wirkvorteil finden sich jedoch gegenüber Clodronat in der MRC-MYELOMA-IX-Studie, in der 1.960 Patienten mit symptomatischem Multiplen Myelom zusätzlich zu definierten Chemotherapieschemata bis zum Fortschreiten der Erkrankung entweder alle drei bis vier Wochen 4 mg Zoledronat i.v.*** erhalten oder täglich 1.600 mg Clodronat einnehmen. Nach medianer Behandlung von 350 Tagen und medianer Nachbeobachtung von 3,7 Jahren wird in einem der primären Endpunkte eine Verlängerung des Überlebens auf im Median 50 Monate gegenüber 44,5 Monaten unter Clodronat errechnet (HR 0,87; 95% CI 0,74-0,96).45 Zoledronat verringert zudem das Risiko skelettbezogener Komplikationen, zu denen in dieser Studie auch neue Osteolysen gerechnet werden, von 35% auf 27% (HR 0,74; 95% CI 0,62-0,87). Auch wenn die neuen Osteolysen nicht berücksichtigt werden, bleibt der Vorteil bestehen. Patienten ohne Knochenläsion bei Studienbeginn (29% der Teilnehmer) profitieren dabei von Zoledronat genauso wie Patienten mit Knochenläsionen (Komplikationsrate: 10% vs. 17% bzw. 35% vs. 43%).46 Zoledronat beurteilen wir deshalb als Mittel der Wahl zur Prophylaxe skelettbezogener Komplikationen bei symptomatischem Multiplem Myelom.
| *** | Bei Niereninsuffizienz wurde die Dosierung gemäß Fachinformation reduziert bzw. die Therapie pausiert. |
Stadien des Multiplen Myeloms
Nach der Klassifikation der internationalen Myeloma Working Group von 2003 wird zwischen asymptomatischem Multiplen Myelom ohne Organschäden und symptomatischem Multiplen Myleom unterschieden, bei dem Organschäden in Form von Anämie, Hyperkalziämie, Niereninsuffizienz, symptomatischer Hyperviskosität, Amyloidose, gehäuften bakteriellen Effekten, Osteolysen oder Osteoporose mit Kompressionsfrakturen bestehen.1 Die Einteilung in die Stadien I bis III nach DURIE und SALMON von 1975, auf die sich die Fachinformationen von Pamidronat (AREDIA, Generika) beziehen, beruht auf Hämoglobin-, Kalzium- und Paraproteinwerten sowie Röntgenbefunden2 und überlappt sich mit der neueren Klassifikation. Patienten im Stadium III würden meist in die Kategorie des symptomatischen Multiplen Myeloms fallen. Inzwischen wird die Stadieneinteilung nach DURIE und SALMON zunehmend vom International Staging System ersetzt, das die Prognose anhand der Beta-2-Mikroglobulin- und Albuminkonzentration abschätzen lässt.3
| 1 | Internat. Myeloma Working Group: Br. J. Haematol. 2003; 121: 749-57 |
| 2 | DURIE, B.G.M., SALMON, S.E.: Cancer 1975; 36: 842-54 |
| 3 | GREIPP, P.R. et al.: J. Clin. Oncol. 2005; 23: 3412-20 |
Bei asymptomatischem Multiplen Myelom finden sich in zwei Studien mit Pamidronat47 und Zoledronat48 keine hinreichenden Belege für einen Nutzen von Bisphosphonaten.
Denosumab ist zur Therapie bei Multiplem Myelom nicht zugelassen. Im direktem Vergleich mit Zoledronat (in der bereits oben erwähnten Studie mit soliden Tumoren außer Brust- und Prostatakrebs und Multiplem Myelom) ist das Sterberisiko bei 180 Patienten mit Multiplem Myelom unter dem Antikörper signifikant höher als unter Zoledronat (HR 2,26; 95% CI 1,13-4,50).24
STÖRWIRKUNGEN: Unter den Bisphosphonaten Pamidronat und Zoledronat ist häufiger als unter Plazebo mit Erbrechen, Atemnot, Müdigkeit, Anämie, Hypokalziämie u.a. zu rechnen. Akute-Phase-Reaktionen mit Fieber und grippeähnlichen Symptomen innerhalb der ersten zwei bis drei Tage nach Infusion treten sehr häufig auf.29 Beide Bisphosphonate können zu Niereninsuffizienz und akutem Nierenversagen führen. Bei schwerer Niereninsuffizienz ist Pamidronat kontraindiziert (Ausnahme: bei lebensbedrohlicher tumorinduzierter Hyperkalziämie) und Zoledronat wird nicht empfohlen.4,7 Im direkten Vergleich wird eine Verschlechterung der Nierenfunktion unter Pamidronat bei 9% und unter Zoledronat bei 11% beobachtet.11 Für die erst nach Markteinführung unter Bisphosphonaten aufgefallenen Kiefernekrosen werden Inzidenzen unter i.v.-Anwendung bei Krebs von 1% bis 19% berichtet. Das Risiko steigt mit der Dauer der Behandlung und ist offenbar unter Zoledronat höher als unter Pamidronat (vgl. a-t 2007; 38: 99-101, 2009; 40: 39).49,50 Bisphosphonate können zudem selten auch schwere Muskel- und Knochenschmerzen auslösen (a-t 2008; 39: 23) und stehen im Verdacht, bei Langzeitanwendung selten zu atypischen Femurschaftfrakturen zu führen (a-t 2010; 41: 117-8).
Das Störwirkungsprofil von Denosumab unterscheidet sich von dem der Bisphosphonate. In Zulassungsstudien bei Knochenmetastasen oder lytischen Läsionen werden Atemnot (21% vs. 18%), Hypokalziämie (18% vs. 9%; schwer 3,1% vs. 1,3%)23 sowie Überempfindlichkeitsreaktionen (5,4% vs. 3,8%) unter dem Antikörper häufiger beobachtet als unter Zoledronat. Denosumab scheint jedoch weniger nephrotoxisch zu sein (9,2% vs. 11,8% unter Zoledronat).25 Nierenversagen wird aber auch unter dem Antikörper bei 5% der Patienten mit vorbestehender mäßiger Niereninsuffizienz (Kreatininclearance![]() 60 ml/min; Zoledronat: 8%) und bei 2,1% der Patienten mit besserer Nierenfunktion (Zoledronat 2,7%) beobachtet.24 Akute-Phase-Reaktionen mit grippeähnlichen Beschwerden innerhalb der ersten drei Tage kommen unter Denosumab weniger häufig vor als unter Zoledronat (7% bis 10% vs. 15% bis 27%).22,32,39
60 ml/min; Zoledronat: 8%) und bei 2,1% der Patienten mit besserer Nierenfunktion (Zoledronat 2,7%) beobachtet.24 Akute-Phase-Reaktionen mit grippeähnlichen Beschwerden innerhalb der ersten drei Tage kommen unter Denosumab weniger häufig vor als unter Zoledronat (7% bis 10% vs. 15% bis 27%).22,32,39
Kiefernekrosen sind mit 1,8% vs. 1,3% unter beiden Mitteln häufig.24***** In einer weiteren Studie tritt die Komplikation unter Denosumab bei 5% der Anwender auf.51 Hinweise auf häufigeres Fortschreiten einer malignen Grunderkrankung aus Studien zum Nutzen von Denosumab bei Knochenverlust unter antihormoneller Therapie von Brust- oder Prostatakrebs (a-t 2010; 41: 60-2) werden in den Studien für fortgeschrittene solide Tumoren nicht erhärtet.
| ***** | Kiefernekrose wird in der Fachinformation von Zoledronat als gelegentlich auftretend (0,1% bis unter 1%) angegeben. |
Schwere unerwünschte Ereignisse werden bei gemeinsamer Auswertung der Vergleichsstudien unter Denosumab insgesamt genauso häufig beobachtet wie unter Zoledronat. In der Studie bei Prostatakarzinom relativieren zusätzliche Ereignisse unter Denosumab (76% vs. 71%)24 aber den potenziellen Vorteil des Antikörpers.
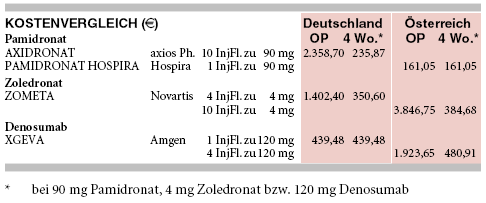
KOSTEN: Zoledronat (ZOMETA) ist mit Kosten von 351 € für 4 mg alle vier Wochen knapp 50% teurer als ein günstiges Pamidronat-Generikum (z.B. AXIDRONAT, 236 € für 90 mg alle vier Wochen). Denosumab (XGEVA) kostet 86% mehr als das Pamidronat-Generikum und 25% mehr als Zoledronat (439 € für 120 mg alle vier Wochen).
Bei Frauen mit Brustkrebs und wenigstens einer osteolytischen Metastase, die Chemotherapie erhalten, mindert Pamidronat (AREDIA) das Risiko skelettbezogener Komplikationen klinisch relevant. Unter gleichzeitiger Hormontherapie ist die Wirksamkeit geringer.
Zoledronat (ZOMETA) bietet bei Brustkrebs keinen Wirkvorteil gegenüber Pamidronat. Ein klinisch relevanter Zusatznutzen von Denosumab (XGEVA) gegenüber Pamidronat ist ebenfalls fraglich. Der Nutzen der Mittel bei ausschließlich nichtosteolytischen Metastasen ist unseres Erachtens nicht hinreichend belegt. Das Risiko für Kiefernekrosen ist unter Zoledronat und Denosumab offenbar höher als unter Pamidronat, weshalb wir Pamidronat hier vorziehen.
Für Ibandronat (BONDRONAT, Generika) ist eine Reduktion des Risikos skelettbezogener Komplikationen bei Brustkrebs weniger sicher belegt, für Clodronat (BONEFOS u.a.) überhaupt nicht.
Bei Knochenmetastasen eines hormonrefraktären Prostatakarzinoms ist Zoledronat Mittel der Wahl zur Prävention skelettbezogener Komplikationen. Denosumab ist zwar mindestens ebenso wirksam, wird aber schlechter vertragen.
Bei anderen soliden Tumoren erachten wir den Nutzen von Bisphosphonaten und Denosumab zur Prophylaxe skelettbezogener Ereignisse als fraglich.
Bei symptomatischem Multiplen Myelom verhindert Zoledronat skelettbezogene Komplikationen und verlängert möglicherweise das Überleben. Es ist hier deshalb Mittel der Wahl.
| (R =randomisierte Studie, M = Metaanalyse) | |
| 1 | COLEMAN, R.E.: Clin. Cancer Res. 2006; 12: 6243s-9s |
| 2 | MELTON III,L.J. et al.: J. Bone Miner. Res. 2004; 19: 25-30 |
| 3 | Bayer: Fachinformation BONEFOS Hartkapseln, Stand Juli 2011 |
| 4 | Novartis Pharma: Fachinformation ZOMETA, Stand Feb. 2012 |
| 5 | Amgen: Fachinformation XGEVA, Stand März 2012 |
| 6 | Roche: Fachinformation BONDRONAT, Stand Juli 2011 |
| 7 | Novartis Pharma: Fachinformation AREDIA, Stand Sept. 2011 |
| R 8 | HORTOBAGYI, G.N. et al.: N. Engl. J. Med. 1996; 335: 1785-91 |
| R 9 | THERIAULT, R.L. et al.: J. Clin. Oncol. 1999; 17: 846-54 |
| 10 | FDA: Medical Review Pamidronate, Stand 20. Sept. 1998 http://www.accessdata.fda.gov/drugsatfda_docs/nda/98/20036s016.cfm |
| 11 | Novartis : US-amerikanische Produktinformation AREDIA, Stand 2010 http://www.accessdata.fda.gov/drugsatfda_docs/label/2011/020036s039lbl.pdf |
| R 12 | ROSEN, L.S. et al.: Cancer J. 2001; 7: 377-87 |
| R 13 | WEINFURT, K.P. et al.: Med. Care 2004; 42: 164-75 |
| 14 | FDA : Medical Review ZOMETA, 22. Feb. 2002; zu finden unter: http://www.accessdata.fda.gov/drugsatfda_docs/nda/2002/21-386_Zometa.cfm |
| 15 | EMA: Europ. Beurteilungsbericht (EPAR) BONDRONAT, Stand 21. Okt. 2005; http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Scientific_Discussion/human/000101/WC500053173.pdf |
| R 16 | BODY, J.J. et al.: Br. J. Cancer 2004; 90: 1133-7 |
| R 17 | BODY, J.J. et al.: Ann. Oncol. 2003; 14: 1399-405 |
| R 18 | ELOMAA, J. et al. Bone 1987; 8 Suppl. 1: S53-6 |
| R 19 | PATERSON, A.H.G. et al.: J. Clin. Oncol. 1993; 11: 59-65 |
| R 20 | KRISTENSEN, B. et al.: J. Intern. Med. 1999; 246: 67-74 |
| R 21 | TUBIANA-HULIN, M. et al.: Bull. Cancer 2001; 88: 701-7 |
| R 22 | STOPECK, A.T. et al.: J. Clin. Oncol. 2010; 28: 5132-9 |
| 23 | Amgen: US-amerikanische Produktinformation XGEVA, Stand Apr. 2012 http://www.accessdata.fda.gov/drugsatfda_docs/label/2012/125320s0054lbl.pdf |
| 24 | EMA: Europ. Beurteilungsbericht (EPAR) XGEVA, 15. Aug. 2011 http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/002173/WC500110384.pdf |
| 25 | Therapeutic Goods Administration: Australian Public Assessment Report for Denosumab, Stand Nov. 2011 http://www.tga.gov.au/pdf/auspar/auspar-xgeva.pdf |
| 26 | VAN POZNAK, C.H. et al.: J. Clin. Oncol. 2011; 29: 1221-7 |
| M 27 | YUEN, K.K. et al.: Bisphosphonates for advanced prostate cancer (Review). The Cochrane Database of Systematic Reviews, Stand 14. Aug. 2006, Zugriff Mai 2012 |
| R 28 | SAAD, F. et al.: J. Natl. Cancer Inst. 2002; 94: 1458-68 |
| 29 | Novartis: US-Produktinformation ZOMETA, Stand März 2012 |
| 30 | EMA: Europ. Beurteilungsbericht (EPAR) ZOMETA, Stand 21. Okt. 2005; http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Scientific_Discussion/human/000336/WC500051691.pdf |
| R 31 | SAAD, F. et al.: J. Natl. Cancer Inst. 2004; 96: 879-82 |
| R 32 | FIZAZI, K. et al.: Lancet 2011; 377: 813-22 |
| 33 | Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF: Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie der verschiedenen Stadien des Prostatakarzinoms, Version 2.0 - 1. Aktualisierung Sept. 2011 (Konsultationsfassung); http://www.urologenportal.de/file admin/MDB/PDF/S3_LL_PCAS3_PCa_Aktualisierung_2011_110912f.pdf |
| R 34 | ROSEN, L.S. et al.: J. Clin. Oncol. 2003; 21: 3150-7 |
| R 35 | ARICAN, A. et al.: Med. Oncol. 1999; 16: 204-10 |
| R 36 | O'ROURKE, N. et al.: J. Clin. Oncol. 1995; 13: 929-34 |
| R 37 | ROBERTSON, A.G. et al.: J. Clin. Oncol. 1995; 13: 2427-30 |
| R 38 | PIGA, A. et al.: J. Exp. Clin. Cancer Res. 1998; 17: 213-7 |
| R 39 | HENRY, D.H. et al.: J. Clin. Oncol. 2011; 29: 1125-32 |
| R 40 | BERENSON, J.R. et al.: N. Engl. J. Med. 1996; 334: 488-93 |
| R 41 | BERENSON, J.R. et al.: J. Clin. Oncol. 1998; 16: 593-602 |
| R 42 | McCLOSKEY, E.V. et al.: Br. J. Haematol. 1998; 100: 317-25 |
| R 43 | LAHTINEN, R. et al.: Lancet 1992; 340: 1049-52 |
| R 44 | HEIM, M.E. et al.: Onkologie 1995; 18: 439-48 |
| R 45 | MORGAN, G.J. et al.: Lancet 2010; 376: 1989-99 |
| R 46 | MORGAN, G.J. et al.: Lancet Oncol. 2011; 12: 743-52 |
| R 47 | D'ARENA, G. et al.: Leuk. Lymphoma 2011; 52: 771-5 |
| R 48 | MUSTO, P. et al.: Cancer 2008; 113: 1588-95 |
| 49 | EMA: CHMP Assessment Report on Bisphosphonates and Osteonecrosis of the Jaw, 24. Sept. 2009; http://www.ema.europa.eu/docs/en_GB/document_library/Report/2010/01/WC500051428.pdf |
| 50 | VAHTSEVANOS, K. et al.: J. Clin. Oncol. 2009; 27: 5356-62 |
| R 51 | SMITH, M.R. et al.: Lancet 2012; 379: 39-46 |
© 2012 arznei-telegramm, publiziert am 7. Mai 2012
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
