Früher auch als CHARCOT'sche Erkrankung bezeichnet, wurde das Krankheitsbild der Multiplen Sklerose (MS) Mitte des 19. Jahrhunderts erstmals
beschrieben. In Deutschland sind etwa 50 bis 60 von 100.000 Einwohnern erkrankt. Die Ursache ist unbekannt. Der chronischen Erkrankung liegt wahrscheinlich
eine autoimmun vermittelte Entzündungsreaktion zu Grunde, die zu einer Zerstörung der Markscheiden des zentralen Nervensystems führt
(Demyelinisierung).
DIAGNOSE UND VERLAUF: Typischerweise beginnt die Multiple Sklerose zwischen dem 20. und 40. Lebensjahr, bei bis zu 5% jedoch bereits vor dem 15.
Geburtstag.1 Frauen erkranken fast doppelt so häufig wie Männer. Die MS verkürzt die Lebenserwartung nach Erhebungen aus den USA
im Mittel um 12 Jahre.2
Bei 85% der Patienten setzt die Erkrankung plötzlich ein. Häufig stehen zu Beginn allgemeine Schwäche, Sensibilitäts- und
Gangstörungen, Optikusneuritis, Augenmuskellähmungen oder Ataxie im Vordergrund. Eine definitive klinische Diagnose erfordert mindestens zwei
Krankheitsepisoden mit zwei oder mehr voneinander unabhängigen Läsionsherden im ZNS. Zur Diagnosesicherung werden Magnetresonanz-
Tomographie (MRT), evozierte Potenziale und Liquorbefunde herangezogen. Kontrastmittelanreicherung im MRT zeigt entzündliche Aktivität an. Die
radiologischen Befunde korrelieren aber nur gering mit dem Ausmaß der klinischen Symptomatik und der zu erwartenden Behinderung.3 Pathologische
Liquorbefunde kommen bei mehr als 75% der Patienten vor. Insbesondere bei Verdacht auf primär progredienten Verlauf mit zunehmenden Beschwerden
über mindestens sechs Monate können sie die Diagnose stützen.
Die internationale Nomenklatur ist nicht einheitlich, dennoch können folgende vier Verlaufsformen unterschieden werden:
 schubförmig remittierende (relapsing-remitting) MS, schubförmig remittierende (relapsing-remitting) MS,
 primär progrediente (primary progressive) MS, primär progrediente (primary progressive) MS,
 sekundär progrediente (secondary progressive) MS, sekundär progrediente (secondary progressive) MS,
 schubförmig progrediente (progressive relapsing) MS.4 schubförmig progrediente (progressive relapsing) MS.4
Bei 80% bis 90% der Patienten verläuft die Erkrankung anfangs schubförmig, bei den übrigen von Beginn an progredient. Mehr als zwei Drittel der
Patienten mit primär schubförmiger MS entwickeln im Verlauf eine sekundär progrediente Erkrankung. Als prognostisch ungünstig gelten
männliches Geschlecht, höheres Alter bei Auftreten der ersten Symptome, Betroffensein mehrerer neurologischer "Systeme" zu
Krankheitsbeginn, hohe Schubfrequenz sowie kurzes Zeitintervall bis zum Erreichen einer mäßiggradigen Behinderung.4
Durchschnittlich vergehen 15 Jahre, bis eine Gehhilfe benötigt wird,5 und 33 bis 35 Jahre, bis die Patienten dauerhaft auf einen Rollstuhl angewiesen
sind.4 Ab einem bestimmten Stadium, wenn etwa eine mäßiggradige Behinderung erreicht ist, verläuft die Erkrankung unabhängig von
der Anzahl der Schübe.6 Dies ist bei der Bewertung der immunmodulierenden Therapien zu berücksichtigen. Für die meisten Verfahren ist
bisher lediglich eine Reduktion der Schubfrequenz nachgewiesen. Der zeitliche Verlauf der Krankheit macht es zudem schwer, Studien so durchzuführen, dass
relevante klinische Veränderungen in die Zeitspanne der Studie fallen (etwa Rollstuhl-Pflicht).
Zur Beurteilung des therapeutischen Nutzens werden meist Skalen, die die klinische Beeinträchtigung bzw. das Ausmaß der Behinderung messen, aber
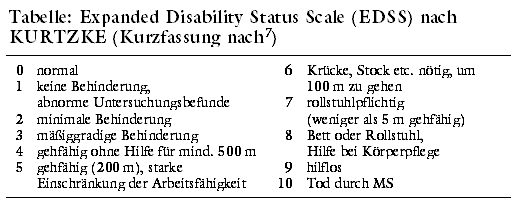
auch Surrogatparameter (MRT u.a.) genutzt. Die am häufigsten verwendete Skala ist die Expanded Disability Status Scale
nach KURTZKE (EDSS) mit Punktwerten von 0 (= normaler neurologischer Status) bis 10 (= Tod im Zusammenhang mit MS; siehe Tabelle). Die Aussagekraft der
Skala ist dadurch eingeschränkt, dass die Gehfähigkeit überbewertet wird und kognitive Beeinträchtigungen, Störungen des
Sehvermögens und Funktionseinschränkungen der oberen Extremitäten zu wenig Bedeutung haben. Der Vorhersagewert kurzfristiger
Änderungen auf der Skala ist nicht ausreichend validiert. Dennoch gilt die EDSS derzeit als das beste Instrument, klinische Veränderungen im Rahmen
von Studien fassbar zu machen. Neue Skalen sind entwickelt, in klinischen Therapiestudien jedoch erst selten verwendet worden.8
Laborparameter und MRT erfüllen bislang nicht die von der FDA gestellten Anforderungen an Surrogatparameter,5 die dann z.B. für
zulassungsrelevante Studien verwendet werden könnten.
THERAPIE: Zu unterscheiden sind die Akutbehandlung und eine langfristige Therapie, die erneuten Schüben und möglichst auch
Behinderungen vorbeugen soll. Standardtherapie des akuten Schubes ist hoch dosiertes Methylprednisolon (URBASON u.a., 500 mg bis 1.000 mg i.v. pro
Tag) über einen Zeitraum von drei bis sieben Tagen. Optimale Dosis und Dauer sind umstritten. Bei der isolierten Neuritis des Nervus opticus kann hoch
dosiertes Methylprednisolon die Dauer des Schubes verkürzen und die Wahrscheinlichkeit senken, innerhalb der nächsten zwei Jahre an manifester
Multipler Sklerose zu erkranken.9
Zur langfristigen Behandlung werden Beta-Interferone (IFN), das Polypeptid Glatiramer (COPAXONE) und das Immunsuppressivum Azathioprin (IMUREK u.a.)
verwendet, ferner andere Immunsuppressiva, Immunglobuline oder Zytostatika, die hierzulande nicht bei MS zugelassen sind.
Interferone (IFN): Derzeit stehen in Deutschland drei Interferon-beta-Präparate zur Verfügung. Das nichtglykosylierte IFN-beta-1b (BETAFERON),
das in Zellkulturen von E. coli erzeugt wird, ist zur Behandlung der schubförmigen und sekundär progredienten MS zugelassen. Die beiden glykosylierten
IFN-beta-1a-Präparate AVONEX und REBIF werden in Ovarialzellen des chinesischen Hamsters synthetisiert und können bei schubförmiger
Verlaufsform verwendet werden. BETAFERON wird üblicherweise jeden 2. Tag subkutan (8 Mio E) gespritzt, 1a-Interferone dreimal wöchentlich subkutan
(REBIF, 22 µg oder 44 µg) bzw. einmal wöchentlich i.m. (AVONEX, 30 µg).
Aus randomisierten kontrollierten Studien zum Nutzen bei schubförmigem Verlauf liegen bisher Daten von rund 1.200 Patienten vor. Die
Beobachtungsdauer beträgt meist zwei Jahre. Die teilnehmenden Patienten haben eine gering- bis mäßiggradige Behinderung (EDSS-Punktwert: 2-3)
und in den zwei Jahren vor Studienbeginn mindestens zwei Schübe. Die Krankheit besteht seit etwa fünf Jahren. Die Schubfrequenz wird durch alle
Beta-Interferone um etwa 30% gesenkt. Dies bedeutet z.B. bei BETAFERON eine absolute Schubsenkung von durchschnittlich 1,27 auf 0,84 pro Jahr.10
Die innerhalb von zwei bis drei Jahren eintretenden EDSS-Veränderungen sind in allen Studien gering, wobei die Interferongruppen etwas besser abschneiden
als die Plazebogruppen.10-12 So werden unter REBIF Verschlechterungen um einen EDSS-Punkt für sieben bis neun Monate
hinausgezögert.11 Der therapeutische Effekt von BETAFERON und AVONEX wird als Rate der Patienten ausgedrückt, bei denen
Veränderungen auf der KURTZKE-Skala von mindestens einem Punkt gemessen werden. Im Vergleich zu Plazebo sind unter Verum 10% (absolute Reduktion)
weniger von einer Verschlechterung betroffen.10,12 Ob eine solche Verzögerung klinische Relevanz für die Patienten hat, ist fraglich.
In Langzeituntersuchungen mit REBIF und BETAFERON scheint der günstige Einfluss auf die Schubrate mit Senkung um etwa 30% auch nach vier
bis fünf Jahren anzuhalten. Die Interferone unterscheiden sich dabei hinsichtlich der Zunahme dauerhafter Behinderungen nicht signifikant von Plazebo. In der
PRISMS*-Studie mit REBIF ergibt sich aber ein Trend zu Gunsten der höheren Dosis. So sind nach vier Jahren unter 44 µg REBIF 56% (97/164) ohne
Krankheitsprogression im Vergleich zu 51% (88/173) unter 22 µg und 46% (74/161) der Patienten aus den ursprünglichen Plazebogruppen, die in der
zweiten Studienhälfte allerdings ebenfalls Verum erhalten (p = 0,07).13 Zu ähnlichen Ergebnissen kommt die Nachbeobachtung der IFNB-Studie
mit BETAFERON.14 Auch hier lässt sich ein Vorteil von BETAFERON nur als Trend dokumentieren.

Die Frage, ob durch frühe Interferontherapie (keine zugelassene Indikation) die Entwicklung einer manifesten MS - definiert als zweiter Schub -
verhindert werden kann, wird in zwei Arbeiten untersucht, in die Patienten bereits nach Auftreten eines ersten Ereignisses und typischer MRT-Veränderungen
eingeschlossen werden.15,16 Unter einmal wöchentlich 22 µg REBIF entwickeln 34% (52/154) der Erkrankten innerhalb von zwei Jahren eine
klinisch manifeste Multiple Sklerose - erleiden also einen zweiten Schub -, unter Plazebo sind es 45% (69/154 p = 0,047).15 Unterschiede der EDSS-Werte
lassen sich nicht nachweisen. Eine vorzeitig abgebrochene Studie mit AVONEX kommt zu ähnlichem Ergebnis.16 Die Arbeiten sagen streng
genommen nur aus, dass IFN auch im Frühstadium der Erkrankung die Schubrate senkt.
An den beiden Studien mit Interferonen bei sekundär progredienter MS17,18 haben über 1.300 Patienten teilgenommen. Ihre Krankheit besteht
seit durchschnittlich 13 Jahren, der mittlere EDSS-Punktwert beträgt 5,1 bis 5,4. BETAFERON verzögert das Fortschreiten der MS innerhalb von
zweieinhalb Jahren um durchschnittlich neun bis zwölf Monate. 39% der Anwender verschlechtern sich in dieser Zeit um einen Punkt auf der KURTZKE-Skala
im Vergleich zu 50% unter Plazebo. Die Teilnehmer der Verumgruppe sind durchschnittlich neun Monate später dauerhaft auf den Rollstuhl angewiesen.17
Diese Ergebnisse werden durch die zweite Studie nicht bestätigt: REBIF senkt innerhalb von drei Jahren zwar die Schubfrequenz, die Zeit bis zur
gesicherten Progression wird jedoch nicht verlängert.18
Vollständig veröffentlichte direkte Vergleiche der Interferone untereinander fehlen. Die so genannte EVIDENCE-Studie soll angeblich Überlegenheit
von REBIF im Vergleich mit AVONEX nachweisen.19 Ob die vollständig publizierten Daten den durch den Studiennamen geweckten hohen
Erwartungen entsprechen werden, bleibt abzuwarten. Gleiches gilt für die vorab veröffentlichten Ergebnisse der INCOMIN-Studie, nach denen
BETAFERON besser abschneiden soll als AVONEX.20
Grippeähnliche Störwirkungen in direktem Zusammenhang mit der Injektion beklagen bis zu zwei Drittel aller Patienten. Zur Linderung wird die
vorherige Einnahme von Parazetamol (BENURON u.a.) empfohlen. Schwere Störwirkungen wie Depression, Suizidalität, Nekrosen an der Einstichstelle
(5%), Kardiomyopathie und Hepatitis kommen vor. Häufig sind Leberwertveränderungen (bis 19%), gastrointestinale Beschwerden (bis 33%),
Kopfschmerzen (bis 84%), Muskelschmerzen (bis 44%) u.a.21 Bis zu 45% der mit BETAFERON behandelten Patienten entwickeln
Antikörper.22 Unter 22 µg bzw. 44 µg REBIF betrifft dies 24% bzw. 14%,23 unter AVONEX 22%12 (vgl. a-t 1996; Nr. 5: 48). Inwieweit diese die klinische Wirksamkeit abschwächen, ist unklar. Von Kreuzreaktionen ist
auszugehen.24
Interferone (IFN) senken die Schubfrequenz um etwa ein Drittel. Dauerhafte Behinderungen bei schubförmigem Verlauf werden allenfalls geringfügig
hinausgezögert. Patienten mit sekundär progredienter Verlaufsform scheinen unter IFN-beta-1b (BETAFERON) im Mittel neun Monate später auf den
Rollstuhl angewiesen zu sein als unter Plazebo. Vollständig veröffentlichte direkte Vergleiche der Interferone untereinander fehlen. Valide Daten für
den optimalen Beginn und die optimale Dauer der Therapie stehen aus.
Glatiramerazetat (COPAXONE, früher Copolymer): Der Wirkmechanismus des synthetischen Polypeptids ist unbekannt. Durch seine Ähnlichkeit
mit Bestandteilen der Myelinscheide sollen T-Zell-vermittelte Entzündungsreaktionen unterdrückt werden. Glatiramerazetat ist nach EU-weiter Zulassung in
Deutschland seit November 2001 auf dem Markt. Täglich müssen 20 mg subkutan injiziert werden.
In einer ersten schon 1987 veröffentlichten kontrollierten Studie mit 50 Patienten sind nach zwei Jahren unter Glatiramer 56% ohne erneuten Schub, unter
Plazebo 26%.25 Dieser außerordentliche Effekt, mit Senkung der durchschnittlichen Schubrate um mehr als 75% (von 2,7 in zwei Jahren auf 0,6), ist
bislang nicht bestätigt worden. In der größten randomisierten zweijährigen Studie mit 251 Teilnehmern wird die Schubfrequenz unter Verum um
ca. 30% reduziert (vgl. a-t 2000; 31: 37). In Verum- und Plazeboarm (EDSS initial durchschnittlich unter 3) erfährt
etwa jeder vierte Teilnehmer eine Progression, mit leichtem Vorteil für Glatiramer (21,6% vs. 24,6%).26 Die Verlängerung der Studie um weitere sechs
Monate bringt gleiche Ergebnisse.27 Eine Nachauswertung neuropsychologischer Testverfahren lässt keinen Vorteil gegenüber Plazebo
erkennen.28 Eine kleine Studie mit 106 Patienten und progredienter Verlaufsform findet keinen signifikanten Einfluss auf das Fortschreiten der MS.29
Häufigste Störwirkung sind lokale Reaktionen an der Einstichstelle wie Schmerz (73%), Pruritus (40%) u.a.30 Bis zu 15% der Patienten
klagen über Kreislaufbeschwerden, Engegefühl in der Brust, Luftnot und Urtikaria in Verbindung mit der Injektion. 3% brechen die Therapie deshalb
ab.26 Die meisten Patienten entwickeln Antikörper, diese sollen die Wirksamkeit des Peptids nicht beeinträchtigen und sich nach drei bis sechs
Monaten zurückbilden.31
Erkenntnisse über Glatiramer aus (veröffentlichten) kontrollierten Studien sind gering. Ähnlich wie die Interferone scheint es die Schubfrequenz
bei Patienten mit mäßiggradiger Behinderung um ein Drittel zu senken. Sein Einfluss auf das Fortschreiten von Behinderungen scheint aber noch geringer
zu sein als der der Interferone. Glatiramer könnte dagegen besser verträglich sein. Da kontrollierte Untersuchungen über mehr als 30 Monate fehlen,
lassen sich Langzeiteffekte nicht beurteilen.
Immunsuppressiva: Azathioprin (IMUREK u.a.) wird seit den 80er Jahren zur Behandlung der MS verwendet, ist hierfür aber in Deutschland erst seit
2000 zugelassen. Laut Fachinformation ist es Mittel der Reserve bei schubförmiger Verlaufsform, "wenn eine Therapie mit Beta-Interferonen nicht
möglich ist oder unter einer bisherigen Therapie mit Azathioprin ein stabiler Verlauf erreicht wurde."
Bisherige Studien sind überwiegend klein. Teilgenommen haben Patienten mit allen Verlaufsformen. In einer 1991 erschienenen Metaanalyse werden sieben
Studien mit insgesamt 739 Patienten ausgewertet. Azathioprin (2-3 mg/kg Körpergewicht [KG]/Tag) senkt die Schubrate gegenüber Plazebo um 30% bis
40%. Das Fortschreiten von Behinderungen wird nicht signifikant beeinflusst.32
Unerwünschte Wirkungen wie Knochenmarkdepression, Pankreatitis, Übelkeit, Erbrechen und allergische Reaktionen führen oft zum
Therapieabbruch. Nach einer Fall-Kontroll-Studie könnte die langjährige Anwendung das Karzinomrisiko von MS-Patienten steigern.33 Statistisch
gesichert ist dieser Verdacht bisher nicht.
In klinischen Studien erprobt ist auch Ciclosporin A (SANDIMMUN u.a.).34,35 Selbst für hohe Dosierungen (7,2 mg/kg KG/Tag) fehlen jedoch
überzeugende Wirksamkeitsbelege. In der größten kontrollierten Studie bricht fast die Hälfte der Ciclosporin-Anwender die Therapie vorzeitig ab,
insgesamt jeder achte wegen der nephrotoxischen und Blutdruck-steigernden Effekte des Mittels.35
Therapieversuche mit Deoxyspergualin (Japan: SPANDIN; vgl. a-t 2000; 31: 85) waren erfolglos.36
Azathioprin reduziert die Schubfrequenz um 30% bis 40%. Ein Einfluss auf das Fortschreiten der Erkrankung ist nicht belegt. Wegen erheblicher
Störwirkungen kommt dem Mittel Reservestatus zu. Für Immunsuppressiva wie Ciclosporin A oder Deoxyspergualin fehlen Nutzenbelege.
Zytostatika: Mitoxantron (NOVANTRON), ein mit dem Anthrazyklin Doxorubicin (ADRIBLASTIN u.a.) verwandtes Zytostatikum, ist seit 2000 in den USA zur
Therapie der MS zugelassen. Der Hersteller Wyeth hat auch in Deutschland die Zulassung hierfür beantragt.
Von den zwei veröffentlichten kontrollierten Studien37,38 mit insgesamt 93 Patienten ist nur eine primär auf Veränderungen nach der
KURTZKE-Skala angelegt: 51 Patienten mit schubförmiger Verlaufsform und EDSS-Wert von durchschnittlich 3,5 erhalten ein Jahr lang einmal monatlich 8
mg/m2 Körperoberfläche (KOF) Mitoxantron. Innerhalb von zwei Jahren verschlechtert sich die MS unter Verum bei 7% um einen Punkt auf der
KURTZKE-Skala im Vergleich zu 37% unter Plazebo. Die durchschnittlichen EDSS-Werte unterscheiden sich dagegen aber zu keinem Zeitpunkt
signifikant.37 Die zweite Studie hat vor allem wegen kurzer Dauer, offener Durchführung und MRT-Befund als primäres Zielkriterium keine
klinische Aussagekraft. An einer dreiarmigen europäischen Multizenter-Studie, die als Zulassungsgrundlage für die FDA gedient haben dürfte, haben
Patienten mit fortgeschrittener Erkrankung (EDSS-Wert 4,5 bis 4,7) teilgenommen. 12 mg oder 5 mg/m2 KOF Mitoxantron alle drei Monate sollen hinsichtlich der
primären Zielparameter wie EDSS-Veränderungen, Anzahl der Schübe u.a. besser wirken als Plazebo.39 Solange die vollständige
Publikation aussteht, lassen sich derartige Angaben aber nicht bewerten.

Sehr häufig wird über Störwirkungen wie Übelkeit, Erbrechen und Haarausfall geklagt. Gefürchtet sind kardiale
Schädigungen in Form von Herzrhythmusstörungen, Kardiomyopathien und Herzinsuffizienz (vgl. a-t 2000; 31:
98). Die Kardiotoxizität nimmt mit Höhe der kumulativen Dosis zu. Auch nach der von der FDA empfohlenen Gesamtdosis von maximal 140 mg/m2
KOF wird lebensbedrohliche Herzinsuffizienz bei bis zu 2,6% der Patienten beobachtet, oft noch Jahre nach Therapieabschluss.21 Langzeitanwendung
scheidet demnach aus.
Der Antimetabolit Methotrexat (LANTAREL u.a.) ist in niedriger Dosierung, wie sie in der Rheumatherapie verwendet wird (einmal wöchentlich 7,5 mg),
auch bei MS untersucht. Zwei randomisierte Studien mit insgesamt 104 Patienten liegen vor. An der größeren haben 60 Patienten mit chronisch
progredienter Verlaufsform (EDSS bei über 60% ( 6) teilgenommen. Unter Verum schreitet die Erkrankung bei 52%, unter Plazebo bei 83% fort. Das signifikante
Ergebnis ist wegen der Kombination verschiedener klinischer Messparameter nicht mit anderen Therapiestudien vergleichbar. Bemerkenswert: Bei Studienende
unterscheidet sich die subjektive Einschätzung der Patienten nicht, je 68% geben an, ihr Zustand habe sich in den letzten zwei Jahren
verschlechtert.40 Die zweite Studie deutet einen Nutzen für Patienten mit schubförmiger, nicht jedoch progredienter MS an. Wegen methodischer
Mängel ist die Untersuchung wenig aussagekräftig.41
Auch unter niedriger Methotrexatdosis ist häufig mit Störwirkungen wie Übelkeit (10%), Durchfall (bis 10%) und
Mundschleimhautentzündungen (bis 3%) zu rechnen. Knochenmarkdepression, Fibrose und Zirrhose der Leber kommen vor. Regelmäßige
Laborkontrollen sind angezeigt.21 Kalziumfolinat-Substitution wird zur Senkung unerwünschter Wirkungen empfohlen.
Der Antimetabolit Cladribin (LEUSTATIN) ist in Deutschland nur zur Behandlung der Haarzell-Leukämie zugelassen. In zwei Studien mit insgesamt 210
Patienten wird er in Dosierungen, die etwa denen zur Leukämiebehandlung entsprechen, bei progredienter MS im fortgeschrittenen Krankheitsstadium (EDSS
4,6 bzw. 5,6) erprobt. Nur die kleinere Studie zeigt einen Effekt, in der größeren schneidet die Plazebogruppe sogar besser ab.42,43 Die
Datenlage für Patienten mit schubförmigem Verlauf ist unzureichend.44
Störwirkungen wie Knochenmarkdepression mit Neutropenie (70%) und Anämie (40%), hohes Fieber (11%), Arthralgie und Myalgie (5-7%)
21 führen zu einer negativen Nutzen-Risiko-Bilanz.
Ebenfalls verwendet wird Cyclophosphamid (ENDOXAN u.a.). In bisherigen Studien, in die meist schwer Erkrankte (EDSS ca. 6) aufgenommen wurden, ist
das Stickstofflost-Analog nur in Kombination mit z.B. ACTH (SYNACTHEN) erprobt.45-47 Widersprüchliche Ergebnisse rechtfertigen nach Ansicht der
MS-Therapie Konsensus Gruppe die Verwendung allenfalls bei schwerem und rasch progredientem Verlauf, wenn andere Therapien ausgeschöpft
sind.48
Unerwünschte Wirkungen wie Übelkeit, Erbrechen, Myelosuppression, hämorrhagische Zystitis und Leberfunktionsstörungen sind
dosisabhängig. Das Blasenkarzinomrisiko scheint bei liegendem Blasenkatheter zuzunehmen.49
Das Anthrazyklin-Zytostatikum Mitoxantron kann unseres Erachtens auf der Basis der bisher veröffentlichten Daten bei Multipler Sklerose nicht empfohlen
werden. Dem fraglichen Nutzen stehen lebensbedrohliche kardiotoxische Effekte entgegen (vgl. a-t 2000; 31: 98).
Einer unserer klinischen Berater hält jedoch die Verwendung bei schwerer Verlaufsform mit rascher Progredienz unter engmaschiger Kontrolle von
Echokardiographie und Laborparametern in Einzelfällen für vertretbar.50 Auch der Antimetabolit Methotrexat kann im Rahmen eines Heilversuchs allenfalls
bei progredienter Verlaufsform erwogen werden, gleiches gilt für Cyclophosphamid bei fortgeschrittener rasch progredienter MS. Für Cladribin sehen wir
keine Indikation.
Immunglobuline: Einmal monatlich verabreichtes Immunglobulin (VENIMMUN u.a.; 0,15 g bis 0,2 g/kg Körpergewicht [KG] i.v.) führt bei 150
Patienten mit schubförmig remittierender MS im zweijährigen Vergleich mit Plazebo zu einem signifikanten, aber klinisch nicht relevanten Unterschied der
EDSS-Werte. Der Ausgangswert von 3.3 nimmt in der Therapiegruppe um 0,2 ab, unter Plazebo um 0,1 zu. Die jährliche Schubfrequenz liegt nach zwei Jahren
unter Verum um die Hälfte niedriger als unter Scheinmedikament (0,42 versus 0,83).51
In einer weiteren Studie erhalten 40 Patienten mit schubförmig remittierender MS zunächst 0,4 g/kg KG/Tag über fünf Tage, in den folgenden
zwei Jahren alle zwei Monate 0,4 g/kg KG oder Plazebo. Die mittlere jährliche Schubrate sinkt unter Immunglobin um 39%, in der Plazebogruppe nur um
4%.52 Zwei randomisierte Studien, in denen Patienten mit lang anhaltender Optikusneuritis bzw. permanentem motorischen Defizit Immunglobuline erhalten
(0,4 g/kg KG), werden erfolglos abgebrochen.36 Das Paul-EHRLICH-Institut hält bisherige Studiendaten nicht für ausreichend, Nutzen und
Sicherheit von Immunglobulinen bei MS nachzuweisen.53
Schwerwiegende unerwünschte Wirkungen sind unter den genannten Dosierungen nicht beschrieben. Neben allergischen Hautreaktionen kommen
Müdigkeit, Kopfschmerzen und erhöhte Temperatur am häufigsten vor. Gefürchtet sind nephrotoxische Störwirkungen. Immunglobuline
gehören zwar zu den relativ sicheren Blutprodukten, ein definitiver Ausschluss der Übertragung infektiöser Erreger ist aber nicht möglich.
I.v.-Immunglobuline senken in maximal zweijährigen Studien die jährliche Schubfrequenz um bis zu 50%, eine klinisch relevante Verzögerung von
Behinderungen ist nicht nachgewiesen. Zur Therapie der MS ist weltweit kein Präparat zugelassen.
Therapiestudien mit weiteren Wirkprinzipien wie Infliximab (REMICADE), Interleukin-10, Lenercept, Linomid (ROQUINIMEX), Sulfasalazin (AZULFIDINE u.a.)
und Transforming growth factor (TGF β2) liefern keinen Nutzenbeleg, führen sogar zu einer erhöhten Schubrate (Lenercept) oder
werden vorzeitig abgebrochen.36
KOSTEN: Für zugelassene Arzneitherapien der MS müssen in Deutschland pro Jahr zwischen 3.000 DM (Azathioprin) und 42.000 DM (REBIF, 44
µg) aufgewendet werden (siehe Kasten). Strittig ist die Finanzierung von Immunglobulinen zu Lasten der GKV.54
 Standardtherapie des akuten Schubes bei Multipler Sklerose ist hoch dosiertes
Methylprednisolon (URBASON u.a.). Standardtherapie des akuten Schubes bei Multipler Sklerose ist hoch dosiertes
Methylprednisolon (URBASON u.a.).
 Die längerfristige immunmodulierende Therapie ist vorwiegend bei Patienten mit
schubförmigem Verlauf und mäßiggradiger Behinderung geprüft. Die längerfristige immunmodulierende Therapie ist vorwiegend bei Patienten mit
schubförmigem Verlauf und mäßiggradiger Behinderung geprüft.
 Zugelassen sind nur Beta-Interferone, Glatiramerazetat (COPAXONE u.a.) und
Azathioprin (IMUREK u.a.). Die am besten geprüften, wenngleich schlecht verträglichen Interferone sind Mittel der ersten Wahl. Zugelassen sind nur Beta-Interferone, Glatiramerazetat (COPAXONE u.a.) und
Azathioprin (IMUREK u.a.). Die am besten geprüften, wenngleich schlecht verträglichen Interferone sind Mittel der ersten Wahl.
 Als gesicherter klinischer Nutzen kann bislang nur die Senkung der Schubfrequenz
um 30% (bis 50%) angesehen werden. Dieser Effekt ist am besten für Beta-Interferone, daneben auch für Glatiramerazetat, Azathioprin und
Immunglobuline belegt. Langzeitdaten bis zu fünf Jahre liegen nur für Interferone vor. Als gesicherter klinischer Nutzen kann bislang nur die Senkung der Schubfrequenz
um 30% (bis 50%) angesehen werden. Dieser Effekt ist am besten für Beta-Interferone, daneben auch für Glatiramerazetat, Azathioprin und
Immunglobuline belegt. Langzeitdaten bis zu fünf Jahre liegen nur für Interferone vor.
 Behinderungen lassen sich nach bisherigen Daten allenfalls geringfügig
hinauszögern, wahrscheinlich höchstens um Monate. Die meisten Erfahrungen liegen auch hier für Interferone vor. Behinderungen lassen sich nach bisherigen Daten allenfalls geringfügig
hinauszögern, wahrscheinlich höchstens um Monate. Die meisten Erfahrungen liegen auch hier für Interferone vor.
 Es fehlen valide Daten zum optimalen Therapiebeginn und zur optimalen
Anwendungsdauer. Kombinationsbehandlung und Wechsel auf andere Therapiestrategien nach Versagen oder Unverträglichkeit eines Prinzips sind nicht
untersucht. Es fehlen valide Daten zum optimalen Therapiebeginn und zur optimalen
Anwendungsdauer. Kombinationsbehandlung und Wechsel auf andere Therapiestrategien nach Versagen oder Unverträglichkeit eines Prinzips sind nicht
untersucht.
 Frühzeitige Interferontherapie (keine zugelassene Indikation) senkt nur die
Schubrate. Effekte auf den Langzeitverlauf der MS sind nicht abzuschätzen. Deshalb ist unseres Erachtens eine konservative abwartende Haltung vertretbar. Frühzeitige Interferontherapie (keine zugelassene Indikation) senkt nur die
Schubrate. Effekte auf den Langzeitverlauf der MS sind nicht abzuschätzen. Deshalb ist unseres Erachtens eine konservative abwartende Haltung vertretbar.
 Bei perakutem Verlauf ist als ultima ratio eine so genannte Eskalationstherapie mit
Mitoxantron (NOVANTRON) oder Cyclophosphamid (ENDOXAN u.a.) im Einzelfall und in spezialisierten MS-Zentren zu erwägen. Bei perakutem Verlauf ist als ultima ratio eine so genannte Eskalationstherapie mit
Mitoxantron (NOVANTRON) oder Cyclophosphamid (ENDOXAN u.a.) im Einzelfall und in spezialisierten MS-Zentren zu erwägen.


|




