Mit einem Erkrankungsgipfel um das 65. Lebensjahr ist das Mammakarzinom die häufigste Krebserkrankung bei Frauen. In den letzten 50 Jahren
haben sich die Neuerkrankungen von 50 auf 100 pro 100.000 Frauen und Jahr verdoppelt. Die Sterblichkeit ist mit 30 pro 100.000 Frauen jedoch konstant
geblieben. Etwa 10% aller Frauen erkranken während ihres Lebens an Brustkrebs. 3,5% sterben daran. Als Hauptrisikofaktor gilt eine positive
Familienanamnese, besonders, wenn eine erstgradig Verwandte frühzeitig betroffen ist. Auch gutartige Brusttumoren bedeuten eine Gefährdung, vor allem,
wenn sie mit atypischen Hyperplasien einhergehen. Ein mäßig erhöhtes Risiko haben Frauen ohne Kinder oder mit Erstgeburten nach dem 30.
Lebensjahr, mit früher Menarche und spät eintretender Menopause, übermäßigem Alkoholgenuß und Hormonersatztherapie jenseits
des 60. Lebensjahres.1
Mehr als die Hälfte der Betroffenen bemerkt zunächst eine knotige, nicht schmerzhafte Verhärtung in der Brust. Jeder zweite Tumor findet sich im
oberen äußeren Quadranten. Etwa 50% der Patientinnen überleben fünf Jahre, die Zehnjahresüberlebensrate liegt bei 30%. Der Verlauf
hängt vor allem von der Größe des Primärtumors und der Zahl der metastatisch befallenen Lymphknoten ab.6
Primär operable Tumoren
LOKALTHERAPIE: Zum Zeitpunkt der Diagnose lassen sich 80% bis 90% der Tumoren operieren. Therapie der Wahl ist heute eine brusterhaltende
Operation mit anschließender Bestrahlung, sofern bestimmte Voraussetzungen (z.B. Einzeltumor, Größe etwa bis 3 cm) erfüllt sind, ferner die
radikale Mastektomie, überwiegend unter Belassung der Pektoralmuskeln (modifiziert). Die Gesamt-Überlebensraten erwiesen sich als
gleichwertig.2-5,7,8,28
Die Entfernung axillärer Lymphknoten unter therapeutischen Gesichtspunkten bleibt umstritten. Der geringeren Rezidivrate stehen häufige
Komplikationen gegenüber, vor allem Schwellungen und Schmerzen im Arm sowie gestörte Beweglichkeit. Die Überlebenszeit bleibt
gleich.2,29 Dennoch wird eine Entnahme überwiegend befürwortet, um Prognose und weitere Therapieplanung besser bestimmen zu
können.10
Nach brusterhaltender Operation gilt eine Nachbestrahlung zumeist noch als unverzichtbar. Bei radikaler oder modifizierter Mastektomie verringert die
postoperative Bestrahlung die örtliche Rezidivrate auf ein Drittel. Die Überlebensraten nehmen dabei langfristig nicht zu, möglicherweise weil mehr
Frauen strahlenbedingt an kardialen Ursachen sterben.2,7,16 Einzelne Studien deuten an, dass eine adjuvante systemische Chemotherapie vor der
postoperativen Nachbestrahlung die Überlebenszeit einiger Patientinnen verlängern kann.2,17,18
ADJUVANTE SYSTEMISCHE THERAPIE: Mammakarzinome bilden frühzeitig Mikrometastasen. Durch verbesserte lokale Behandlung lässt sich
die Lebenserwartung daher nicht weiter verlängern. Nach einer Metaanalyse von 133 randomisierten Studien mit 75.000 Patientinnen erhöhen adjuvante
systemische Behandlungen sowohl die rezidivfreien als auch die Gesamtüberlebensraten über 10 bis 15 Jahre,9 in einer Untersuchung auch
über 20 Jahre.15 Sind Achsellymphknoten befallen, erscheinen die Erfolge deutlicher als bei Begrenzung des Tumors auf die Brust.6
Ob die unterstützende systemische Therapie die Heilungschancen beim Mammakarzinom tatsächlich erhöht oder lediglich die Zeit bis zum Auftreten
eines Rückfalls verlängert, bleibt offen. Adjuvante Maßnahmen senken vor allem die Rate von Lokal- und Weichteilrezidiven. Die für die
Prognose bedeutsameren Knochen- und Organmetastasen lassen sich weniger beeinflussen.19 Auf der großen Metaanalyse sowie einer
Aktualisierung12 von 1995 beruhen pragmatische Therapieempfehlungen:10
Alle Frauen mit befallenen Achsellymphknoten sind adjuvant zu behandeln. Vor den Wechseljahren gilt unabhängig davon, ob der Tumor
Hormonrezeptoren aufweist, eine Polychemotherapie als Verfahren der Wahl. Sie erhöht den Anteil krankheitsfreier Patientinnen aller Altersstufen
nach 10 Jahren um 9% auf 39% und die Gesamtüberlebensrate um 7% auf 47%, wobei Frauen vor der Menopause stärker profitieren (10% vs. 5%).
Standard sind sechs Zyklen eines CMF-Schemas (Cyclophosphamid [ENDOXAN u.a.], Methotrexat [METHOTREXAT
"LEDERLE" u.a.], Fluorouracil [5-FU LEDERLE u.a.]) über sechs Monate. Alternativ kommen vier Zyklen des AC-Schemas
(Adriamycin [= Doxorubicin, ADRIBLASTIN u.a.], Cyclophosphamid) über drei Monate in Betracht. Wegen
ausgeprägter Kardiotoxizität von Anthrazyklinen wie Doxorubicin (a-t 12 [1996], 123) wird bei kardialen
Begleit- oder Vorerkrankungen sowie linksthorakaler Vorbestrahlung das CMF-Schema bevorzugt. Niedrigere als die empfohlenen Dosierungen verringern den Erfolg
der Polychemotherapie.
Weist der Tumor Hormonrezeptoren auf, wird jetzt auch eine Ovarektomie als Alternative zur Polychemotherapie akzeptiert.14 Innerhalb von 10
Jahren erhöht sie den Anteil der Frauen, die rezidivfrei überleben, um 13% auf 50% und die Überlebensrate insgesamt um 10% auf 57%.9
Ovarielle Suppression mit LHRH-Analoga gilt als nicht ausreichend untersucht. Möglicherweise profitieren einige Frauen von einer Kombination von
Chemotherapie und Ovarektomie. Hochdosis-Chemotherapie mit anschließender autologer Blutstammzell-Reinfusion bei Hochrisiko-Patientinnen mit
mindestens zehn befallenen axillären Lymphknoten bleibt spezialisierten Zentren unter vergleichenden Studienbedingungen vorbehalten. Die therapiebedingte
Sterblichkeit liegt bei 3%.
Nach den Wechseljahren nehmen Frauen mit axillärem Lymphknotenbefall und Nachweis von Östrogenrezeptoren das Antiöstrogen
Tamoxifen (NOLVADEX u.a., 20 mg bis 30 mg/Tag) ein. Bei negativem Rezeptorstatus erhalten sie eine Polychemotherapie. Regime und Dosierungen
entsprechen den Empfehlungen bei Frauen vor der Menopause und sind trotz des höheren Alters der Patientinnen nach Möglichkeit einzuhalten. Die
Kombination von Tamoxifen mit dem CMF-Schema verbessert die Überlebenszeiten nicht wesentlich, verschlechtert aber die
Lebensqualität.13
Tamoxifen wirkt offenbar nicht nur antiöstrogen, sondern besitzt noch andere antitumoröse Effekte.22 In überwiegend mit Frauen nach der
Menopause durchgeführten Untersuchungen erhöht es die rezidivfreie Überlebensrate um 9% auf 42% in 10 Jahren und die
Gesamtüberlebensrate um 8% auf 50%. Die optimale Behandlungsdauer ist nicht bekannt, sie soll aber mindestens zwei Jahre betragen. Mehr als
fünfjährige Einnahme bringt keinen zusätzlichen Nutzen (a-t 1 [1996], 14).11
Störwirkungen wie Völlegefühl, Hitzewallungen, Gesichtsröte und Trockenheit von Haut und Schleimhäuten werden meist
toleriert.32 Das Antiöstrogen erhöht abhängig von Dosis und Behandlungsdauer das Risiko eines Endometriumkarzinoms bis auf das
Dreifache (a-t 5 [1994], 48).31 Die Vorteile der unterstützenden Behandlung mit Tamoxifen
überwiegen jedoch.
Für über 70jährige gilt Tamoxifen als Adjuvans der Wahl. Eine Polychemotherapie ist allenfalls alternativ bei Tumoren ohne
Östrogenrezeptor zu erwägen, wenn sie ohne Dosisreduktion durchführbar ist.
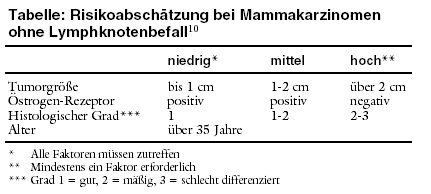
Für Patientinnen ohne axilläre Lymphknotenmetastasen sind die Empfehlungen weniger gut durch klinische Studien abgesichert. Anhand von
Alter, Größe des Primärtumors, Rezeptorstatus und histologischer Differenzierung ist zunächst das individuelle Risiko zu ermitteln (siehe Tabelle).
Ist dieses niedrig, liegt die Wahrscheinlichkeit eines Rezidivs innerhalb von zehn Jahren unter 10%.12 Eine adjuvante Behandlung ist in der Regel nicht
angebracht. Der Stellenwert einer Therapie mit Tamoxifen ist Gegenstand klinischer Studien. Für Patientinnen mit mittlerem Risiko kommt Tamoxifen in Betracht.
Klinische Studien vergleichen den Nutzen des Antiöstrogens bei Frauen vor den Wechseljahren derzeit mit Ovarektomie oder Polychemotherapie. Bei hohem
Risiko gelten die gleichen Empfehlungen wie bei befallenen Achsellymphknoten.
Fortgeschrittenes Mammakarzinom
Bei Frauen mit fortgeschrittenem Mammakarzinom (Rezidive, primäre Fernmetastasen oder inoperable Tumoren) bleibt eine langfristige Erhaltung,
möglichst Verbesserung von Befinden und Leistungsfähigkeit oberstes Ziel. Die durchschnittliche Überlebenszeit von 18 bis 24 Monaten nach dem
Auftreten von Metastasen lässt sich meist nicht verlängern.20,21
Beim in die oberflächlichen Lymphgefäße metastasierten sog. inflammatorischen Brustkrebs hat sich eine anfängliche Chemotherapie, gefolgt
von Mastektomie und/oder Nachbestrahlung, bewährt.6 Sonst werden inoperable Mammakarzinome oder Lokalrezidive in der Regel zunächst
bestrahlt. Um Fernmetastasen einzudämmen und die Wirksamkeit der Strahlentherapie zu verbessern, folgt meist eine systemische
Therapie.27
ENDOKRINE THERAPIE: Für die meisten Frauen eignet sich zunächst eine endokrine Behandlung, die östrogene Effekte an den
Tumorzellen verringern soll. Bei geringer Gesamt-Tumormasse, Überwiegen von Weichteil- und Knochenmetastasen, wenigen oder fehlenden Organmetastasen
und bei Rezidiven nach mehr als 24 Monaten bietet sie gute Erfolgsaussichten. Zwischen 50% und 70% der Frauen mit positiven Hormonrezeptoren sprechen an, bei
unbekanntem Rezeptorstatus 30% bis 40%.21,22 Bei Erfolg wird die Therapie bis zur erneuten Progression weitergeführt, meist 9 bis 12 Monate. Die
Hälfte der Frauen profitiert dann auch von weiteren endokrinen Verfahren.
Vor der Menopause stehen LHRH-Analoga im Vordergrund, z.B. subkutane Depotinjektionen von Goserelin (ZOLADEX, 3,6 mg alle vier Wochen).
Sie unterdrücken die ovarielle Östrogenbildung. Wegen der Reversibilität werden LHRH-Analoga besser akzeptiert als die Entfernung der
Eierstöcke. Neben Zeichen des Östrogenentzugs ist mit Übelkeit, Blutdruckabfall, Depressionen und Schlafstörungen zu rechnen.25
Spricht die Patientin anfänglich auf LHRH-Analoga oder Ovarektomie an, kommt bei erneutem Fortschreiten Tamoxifen zum Zuge. Eine Behandlung mit
LHRH-Analoga soll dabei weitergeführt werden. Der Nutzen dieser Empfehlung ist allerdings nicht belegt.
Nach den Wechseljahren gilt Tamoxifen als endokrine Therapie der Wahl. Ovarektomie oder ovarielle Suppression mit LHRH-Agonisten bieten hier keine
Erfolgsaussichten.
Vergleichsuntersuchungen von Tamoxifen mit anderen endokrinen Behandlungsformen liegen für die Initialtherapie nach den Wechseljahren und die
Folgetherapie vor der Menopause erst begrenzt vor. Droloxifen und das kürzlich für Frauen nach den Wechseljahren zugelassene Toremifen
(FARESTON) sind Struktur-Analoga von Tamoxifen mit geringeren agonistischen Effekten am Östrogen-Rezeptor. Die antiöstrogene Wirkung entspricht
der von Tamoxifen.22
Schreitet die Erkrankung unter Tamoxifen erneut fort, erhalten Frauen vor und nach der Menopause eine weitere endokrine Behandlung. Welche dann am
besten wirkt, ist bisher nicht ausreichend untersucht. Wegen relativ besserer Verträglichkeit werden nahezu einheitlich Aromatasehemmer
empfohlen.20-22 Sie vermindern in nicht ovariellen Geweben die Umwandlung von Androgenen in Östrogene, dem Hauptsyntheseweg von
Östrogenen nach den Wechseljahren. Vor der Menopause sind sie nur nach Entfernung der Eierstöcke oder in Kombination mit LHRH-Analoga
angezeigt.
Aminoglutethimid (ORIMETEN u.a.) ist ein unspezifischer Aromatasehemmer, der in den Nebennieren auch die Synthese anderer Hormone wie Cortisol vermindert.
Nach neueren Empfehlungen reichen 250 mg bis 500 mg täglich aus, wodurch die früher nach höheren Dosierungen übliche Cortisol-
Substitution entfallen kann und Störwirkungen wie Somnolenz und Hautausschlag seltener auftreten sollen.6,21
Der steroidale selektive Aromatasehemmer Formestan (LENTARON DEPOT) beeinträchtigt auch in höherer Dosierung die Hormonsynthese in der
Nebenniere nicht wesentlich. Nach indirekten Vergleichen mit Aminoglutethimid wirkt Formestan etwa gleich gut, soll aber besser vertragen werden. Neben
Lokalreaktionen (15%) treten systemische Störwirkungen wie Brechreiz, Hautausschlag, Schläfrigkeit, Gesichtsröte, Krämpfe und Haarausfall
bei 12% der Frauen auf, anaphylaktoide Reaktionen bei 2%. Direkte Vergleiche mit Aminoglutethimid und Gestagenen sowie Untersuchungen zur
Lebensqualität fehlen. Die dreifach höheren Kosten lassen eine Anwendung (alle zwei Wochen 250 mg intramuskulär) nur gerechtfertigt erscheinen,
wenn Aminoglutethimid nicht vertragen wird.23,24
Anastrozol (ARIMIDEX), das soeben eingeführte Letrozol (FEMARA) und Fadrazol (Japan: AFEMA) sind nicht-steroidale Hemmstoffe der Aromatase ohne
relevanten Einfluss auf die Hormonsynthese in der Nebenniere. Störwirkungen wie Übelkeit, Erbrechen und Durchfall treten bei bis zu 30% der
Anwenderinnen auf, Schwächegefühl, Kopfschmerz und Hitzewallungen bei bis zu 15%.30 Anastrozol und Letrozol sind im Vergleich zu Aminoglutethimid
bis zu zweieinhalbfach teurer (vgl. Kasten), ohne belegbar Vorteile zu bieten. Bislang unveröffentlichte Pilotstudien mit Letrozol und Aminoglutethimid lassen eine
gleiche Wirksamkeit annehmen, belegen jedoch keinen Vorteil für Letrozol. Die optimale Dosis der Neuerung steht noch nicht fest.33
Hochdosierte Gestagene kommen bei fortgeschrittenem Mammakarzinom mit erneuter Progression unter Aromatasehemmern in Betracht.20,21 Ihre
Wirkung beruht vor allem auf vermehrter Umwandlung von Estradiol in das wirkschwächere Östron sowie auf verminderter Ausbildung (Expression) von
Östrogen-Rezeptoren. Zur Verfügung stehen Megestrol (MEGESTAT, 160 mg/Tag) und Medroxyprogesteron (CLINOVIR u.a., 250 mg bis 1.000 mg/Tag).
Beide wirken etwa gleich gut wie Aromatasehemmer, bleiben aber wegen ihrer relativ schlechten Verträglichkeit mit Bluthochdruck, Salz- und Wasserretention,
Hyperglykämie, Hirsutismus und Thromboembolie in der Reserve. Positiv erscheint die häufige Gewichtszunahme infolge
Appetitsteigerung.22

ZYTOSTATISCHE BEHANDLUNG: Wirken endokrine Verfahren von Beginn an nicht oder entwickelt sich unter der Behandlung eine Resistenz, wird
auf Zytostatika zurückgegriffen. Bei jungen Frauen mit rasch progredientem Verlauf, fehlenden Östrogenrezeptoren oder Rezidiv nach weniger als 24
Monaten können sie auch primär erforderlich sein, insbesondere wenn lebensbedrohliche Komplikationen wie ausgedehnte Lebermetastasen auftreten.
Bestehen Organmetastasen, wirken Zytostatika besser als endokrine Verfahren. Für ältere Patientinnen mit langsamem Krankheitsverlauf bringt ihr
früher Einsatz Nachteile.20
40% bis 50% der Frauen sprechen auf Zytostatika an. Die Wirkung hält sechs bis zehn Monate an.22 Schlägt die erste zytostatische Therapie
nicht an, liegen die Erfolge folgender Behandlungen oft unter 25%. Polychemotherapien erzielen höhere Ansprechraten als Monotherapien, ohne jedoch die
Überlebenszeit zu verlängern.6
Zunächst wird meist das CMF-Schema gewählt. Anthrazyklin-haltige Kombinationen (AC-Schema mit oder ohne Fluorouracil) wirken schneller und bei mehr
Frauen, werden aber wegen häufiger Störwirkungen primär nur bei rasch fortschreitender Organmetastasierung bevorzugt. Bei Resistenz gegen das
CMF-Schema lohnt ein Wechsel auf das AC-Schema und umgekehrt. Wirkt eine Polychemotherapie, ist sie bis zur deutlichen Linderung bzw. Stabilisierung der
Symptome fortzuführen, aber nicht zwingend bis zur erneuten Krankheitsprogression. Meist liegt die Behandlungsdauer zwischen 6 und 12 Monaten.
Die Hochdosis-Chemotherapie mit anschließender peripherer Knochenmarkstammzell-Reinfusion wird in Studien auch bei fortgeschrittenem Mammakarzinom
erprobt. Trotz häufigerer Vollremissionen lassen sich bislang keine Überlebensvorteile erkennen.20,25
Schreitet die Erkrankung nach dem ersten oder zweiten Polychemotherapie-Regime erneut fort, können Mitomycin C (MITO-MEDAC u.a.), Vindesin
(ELDISINE), Etoposid (VEPESID), Ifosfamid (HOLOXAN) und Mitoxantron (NOVANTRON u.a.), meist in Kombinationsregimen, noch wirken. Die Ansprechraten
liegen selten über 10%.
Besteht Resistenz gegen Zytostatika, insbesondere Anthrazykline, lassen sich mit den Eibenrindenabkömmlingen Paclitaxel (TAXOL, a-t 10 [1993], 96) und Docetaxel (TAXOTERE) noch Ansprechraten bis zu 25% erzielen. Wegen erheblicher
Störwirkungen, z.B. schwere Neutropenie und Schädigung des Herzmuskels, sowie immenser Kosten von etwa 6.000 DM monatlich kommen sie nur
ausnahmsweise in Betracht. Auf die Überlebenszeit haben auch sie keine nachgewiesene Wirkung.26
FAZIT: Jede zehnte Frau erkrankt während ihres Lebens an Brustkrebs. Operable Tumoren werden durch brusterhaltende Operation mit
anschließender Bestrahlung entfernt, seltener durch Mastektomie und dann überwiegend unter Belassung der Pektoralmuskulatur. Die Entnahme der
Achsellymphknoten dient vor allem der weiteren Therapieplanung.
Nahezu alle Frauen erhalten eine adjuvante systemische Therapie. Abhängig davon, ob die Wechseljahre eingetreten sind und der Tumor Hormonrezeptoren
aufweist, kommen Polychemotherapie, Ovarektomie oder das Antiöstrogen Tamoxifen (NOLVADEX u.a.) in Betracht.
Ist das Mammakarzinom fortgeschritten, lässt sich die Überlebenszeit kaum verlängern. Erhalt der Lebensqualität und Verträglichkeit der
Therapie treten in den Vordergrund. Neben einer abgestuften endokrinen Behandlung mit LHRH-Agonisten, Tamoxifen, Aromatasehemmern oder hochdosierten
Gestagenen finden Mono- und Polychemotherapien mit verschiedenen Zytostatika Verwendung.

|



