INSULTPROPHYLAXE BEI VORHOFFLIMMERN
... ASS und CHADS2-Score noch zeitgemäß?
Bis dato erfolgte die Risikobeurteilung in Bezug auf einen Apoplex bei Vorhofflimmern mittels CHADS2-Score. Hier wurde im Hinblick auf das ermittelte Risiko zwischen Prävention mit ASS oder MARCUMAR entschieden. Jetzt habe ich gelesen, dass eine Therapie mit ASS bei niedrigem Risiko nicht mehr zeitgemäß sein soll, da es für ASS keine Wirksamkeitsbelege gäbe. Frage: Gibt es tatsächlich keine Daten in Bezug auf ASS und Apoplexie bei Vorhofflimmern? Wie valide ist der empfohlene CHA2DS2-VASc-Score?
S. BÖNIG (Facharzt für Innere Medizin)
D-38640 Goslar
Interessenkonflikt: keiner
ASS BEI VORHOFFLIMMERN: Bei Patienten mit nichtvalvulärem Vorhofflimmern senkt Azetylsalizylsäure (ASS; ASPIRIN, Generika) gegenüber Plazebo oder Nichtbehandlung die Rate von Insulten jeder Genese nach Daten aus Metaanalysen randomisierter kontrollierter Studien relativ um 19% bis 30%.1-4 Werden nur Patienten mit transitorischer ischämischer Attacke (TIA) oder Insult in der Anamnese berücksichtigt, fällt die Reduktion der Insultrate signifikant aus,1,2 während die Ergebnisse bei Patienten ohne TIA oder Insult knapp nicht signifikant sind.3,4
Bei 1.000 Patienten ohne TIA oder Insult verhindert ASS 8 Insulte pro Jahr, bei 1.000 Patienten mit TIA oder Insult 25 (siehe Tabelle 1).1 Schwere extrakranielle Blutungen nehmen
unter ASS unabhängig von einer Insult-Anamnese um 60% zu,2 entsprechend 2-3 pro 1.000 Patientenjahre.1,2 ASS hat keinen nachgewiesenen Einfluss auf die Mortalität.1-4

Cumarin-Antikoagulanzien (INR 2-3) sind ASS (75-325 mg/Tag) in dieser Indikation überlegen: Bei Patienten mit nichtvalvulärem Vorhofflimmern ohne TIA oder Insult in der Anamnese reduzieren sie Insulte jeder Ätiologie im Vergleich zu ASS signifikant um 32% und systemische Embolien um 52%. Hirnblutungen und schwere extrakranielle Blutungen sind allerdings fast doppelt so häufig.5 Pro 1.000 Patienten treten unter oraler Antikoagulation pro Jahr 12 ischämische Insulte weniger, aber 8 schwere Blutungen mehr auf als unter ASS.6 Bei Patienten mit oder ohne TIA oder Insult vermindern Cumarine im Vergleich zu Thrombozytenaggregationshemmern Insulte jeder Genese um 38% bis 52%. Schwere extrakranielle Blutungen nehmen jedoch um 42% bis 71% zu.1,2,6 Pro 1.000 Patienten treten unter Cumarinen in diesem Kollektiv jährlich 23 ischämische Insulte weniger und 9 schwere Blutungen mehr auf. Werden nur Patienten mit TIA oder Insult betrachtet, stehen 60 verhinderten Insulten 15 zusätzliche schwere Blutungen gegenüber.6
Für Patienten mit nichtvalvulärem Vorhofflimmern ohne TIA oder Insult in der Anamnese scheint ein Nutzen von ASS somit unsicher und allenfalls begrenzt. Patienten mit TIA oder Insult profitieren zwar von ASS, jedoch eindeutig geringer als von Cumarinen. In den ursprünglichen Studien zu Nutzen und Schaden von ASS bei Vorhofflimmern fanden andere Risikofaktoren als TIA und Insult, die vom CHADS*2-Score7 und CHA2DS2-VASc*-Score8 mit erfasst werden, keine Verwendung und wurden auch nicht systematisch erhoben.9 Eine an solchen Risikofaktoren orientierte Verordnung von ASS ist somit in Studien nicht geprüft.
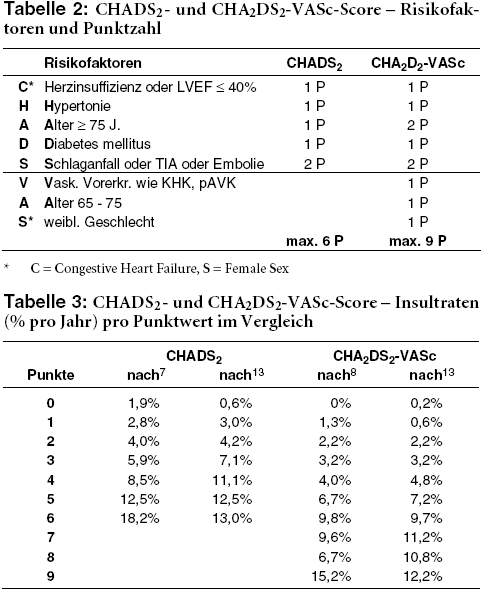
| * | CHADS2-Score, CHA2DS2-VASc-Score: Scores zur Einschätzung des Insultrisikos bei Vorhofflimmern, siehe Tabelle 2. |
In Leitlinien wird ASS nur noch bei Patienten ohne weitere Risiken (CHADS2-Score = 0) empfohlen - und dann nachrangig zu keiner antithrombotischen Therapie - oder bei maximal einem Risikofaktor wie Herzinsuffizienz, Diabetes, Hypertonus oder Alter ≥ 75 Jahre (CHADS2-Score = 1) und dann nachrangig zur oralen Antikoagulation.2,10-12 Die gerade aktualisierte europäische Leitlinie sieht kein Indikationsgebiet mehr für ASS bei nichtvalvulärem Vorhofflimmern und hält die Anwendung nur für angebracht, wenn Patienten bei gegebener Indikation für orale Antikoagulanzien diese strikt ablehnen - und dann auch nur nachrangig zu ASS plus Clopidogrel (PLAVIX, Generika, vgl. a-t 2006; 37; 67 und 2009; 40: 45-6).9 Begründet wird dies damit, dass das Blutungsrisiko unter ASS so hoch sein soll wie unter oralen Antikoagulanzien. Solche Daten stammen aber überwiegend aus Beobachtungsstudien13,14 und sind dadurch verzerrt, dass in der Praxis gerade bei erhöhtem Blutungsrisiko im Zweifel eher ASS als Antikoagulans verwendet wird ("confounding by indication").
VALIDITÄT DES CHA2DS2-VASC-SCORE: Der CHA2DS2-VASc-Score8 ist eine Weiterentwicklung des vor gut zehn Jahren anhand epidemiologischer Daten nicht antikoagulierter Patienten mit nichtvalvulärem Vorhofflimmern entwickelten CHADS2-Score.7 Bei einem CHADS2-Score von 2 lag das Insultrisiko in der ursprünglichen Validierung bei 4% pro Jahr.7 Seit Jahren wird dieser Wert in den gängigen Leitlinien als sichere Interventionsschwelle für orale Antikoagulanzien akzeptiert, sofern nicht das individuelle Blutungsrisiko des Patienten dagegen spricht.2,10-12 Der CHADS2-Score ist gut bekannt und leicht anwendbar. Er wird aber zunehmend kritisiert, da er einige Risikofaktoren nicht berücksichtigt und das Insultrisiko insgesamt nur mäßig genau vorhersagt.15,16 Während er bei Werten ab 2 für therapeutische Entscheidungen ausreichend diskriminiert, soll er vor allem bei Werten von 0 und 1 (jährliches Insultrisiko im Mittel 0,6% bis 1,9% bzw. 2,8% bis 3,0%) die Patienten, die sicher keiner antithrombotischen Behandlung bedürfen, nur unzureichend erkennen.8-10 Hier soll der CHA2DS2-VASc-Score weiter helfen. Er berücksichtigt als zusätzliche Risikofaktoren Alter zwischen 65 und 74 Jahren, weibliches Geschlecht sowie koronare oder periphere Gefäßerkrankung und gewichtet ein Alter ≥ 75 Jahre doppelt so stark wie der CHADS2-Score.8
Ursprünglich wurde der CHA2DS2-VASc-Score an einem relativ kleinen britischen Kollektiv validiert.8 Seine bessere Diskriminierung des Insultrisikos in einem Bereich, der nach dem CHADS2-Score (0-1) als niedrig bis mäßig eingestuft wird, wurde aber an einem schwedischen Kollektiv mit mehr als 90.000 nicht antikoagulierten Patienten bestätigt (Tabelle 3).13,17 Dies bekräftigen auch dänische Registerdaten von 47.000 nicht antikoagulierten Patienten mit CHADS2-Score-Werten zwischen 0 und 1: Bei einem Wert von 0 liegt die Insultrate ohne Antikoagulation bei 1,3% pro Jahr. Im CHA2DS2-VASc-Score entspricht dies Werten von 0 bis 3 und Insultraten von 0,8% bis 2,1%. Bei einem CHADS2-Score von 1 mit einer Insultrate von 3,6% pro Jahr differenziert der CHA2DS2-VASc-Score in Werte von 1 bis 4 und Insultraten von 1,5% bis 4,9%.18
Auch der CHA2DS2-VASc-Score wird kritisch beurteilt.17 Über den gesamten Risikobereich bietet er keine wesentliche Verbesserung im Vergleich zum CHADS2- oder anderen Scores zur Vorhersage des Insultrisikos.13 Die Validierungsstudien verdeutlichen zudem, dass nicht alle im Score gleich bepunkteten Faktoren das Insultrisiko in gleichem Maße erhöhen. TIA, Insult oder systemische Embolie in der Anamnese sowie Alter von mindestens 75 Jahren erhöhen das Insultrisiko konsistent am stärksten und in ähnlichem Maße. Auch Alter zwischen 65 und 74 Jahre sowie Diabetes steigern das Risiko konsistent und vergleichsweise deutlich. Weniger konsistent und teils widersprüchlich ist dagegen, inwieweit Herzinsuffizienz und Hypertonus und vor allem koronare oder periphere Gefäßleiden und weibliches Geschlecht unabhängige Risikofaktoren darstellen.8,13,19-21 Frauen haben nur im Alter ein höheres Risiko als Männer. Bei unter 65-Jährigen ist weibliches Geschlecht allein kein Risikofaktor,21-23 ebensowenig wie eine nur anamnestisch bekannte Herzinsuffizienz.13 Dagegen scheint eine chronische Niereninsuffizienz ein bisher in Scores nicht erfasster Risikofaktor für Insulte bei Vorhofflimmern zu sein.24
Ob der CHA2DS2-VASc-Score praxistauglich ist, muss noch bewiesen werden.17,25 In US-amerikanische Leitlinien hat er bisher keinen Eingang gefunden.2,12,26 Die kanadische Leitlinie diskutiert ihn eingehend, richtet die Therapieempfehlungen aber wie die US-amerikanischen weiter am CHADS2-Score aus. Nur bei einem Wert von 0 zieht sie die Risikofaktoren heran, die durch den CHA2DS2-VASc-Score zusätzlich erfasst werden und rät bei einem Alter von mindestens 65 Jahren oder bei weiblichem Geschlecht plus Gefäßleiden zur oralen Antikoagulation.11
Ganz im Gegensatz zu den amerikanischen rät jetzt die aktualisierte europäische Leitlinie, wesentlich vom Verfasser des CHA2DS2-VASc-Score8 mitgestaltet, dezidiert von der weiteren Verwendung des CHADS2-Score zu Gunsten des neueren Scores ab.9 Sie spricht sich zudem explizit für eine Ausweitung der Indikation für orale Antikoagulanzien aus: Sie sollen ab einem CHA2DS2-VASc-Score von 1 verordnet werden, solange weibliches Geschlecht nicht der einzige Risikofaktor ist, während ASS - bis auf die oben genannte Ausnahme - gar nicht mehr empfohlen wird. 95% aller Patienten mit nicht valvulärem Vorhofflimmern und 85% mit einem CHADS2-Score von 0 bis 1 müssten dann orale Antikoagulanzien erhalten.17,18 Gäbe man eine Interventionsschwelle von 2 Punkten für beide Scores vor, würde sich durch Verwendung des CHA2DS2-VASc- statt des CHADS2-Score die Zahl der zu antikoagulierenden Patienten verdoppeln.27 Bedenkt man ferner, dass die europäische Leitlinie den neuen oralen Antikoagulanzien (Dabigatran [PRADAXA, a-t 2011; 42: 74-7 u. 103-4], Rivaroxaban [XARELTO; a-t 2012; 43: 11-2] und bei Verfügbarkeit auch Apixaban [ELIQUIS; a-t 2011; 42: 59-60]) gegenüber Cumarinen eine Präferenz einräumt, kann an der Unabhängigkeit ihrer Empfehlungen gezweifelt werden.
Wir halten den CHADS2-Score weiter für ein einfaches und bewährtes Instrument, um Patienten mit klarer Indikation für orale Antikoagulanzien zu erkennen (Werte ≥ 2). Bei Score-Werten von 0 bis 1 kann das Insultrisiko mit dem CHA2DS2-VASc-Score offenbar genauer eingeschätzt werden: Der Punktwert entspricht hier in etwa dem prozentualen Jahresrisiko. Er kann dann eine Hilfe bei der Indikationsstellung für orale Antikoagulanzien sein. Bei der individuell mit dem Patienten zu treffenden Entscheidung sollte aber Risiken wie Alter und Diabetes ein besonderes Gewicht beigemessen werden.
Zur Abschätzung des Risikos für schwere Blutungen kann der HAS-BLED**-Score mit heran gezogen werden.28 Einige der berücksichtigten Faktoren sind identisch mit denen des CHADS2-Score. Obwohl ebenfalls nicht unumstritten,17 hat er in Validierungsstudien an größeren Kollektiven eine ausreichende Vorhersagekraft für schwere und intrakranielle Blutungen gezeigt, sowohl bei Patienten mit als auch ohne ASS oder Antikoagulation.13,29,30 Wichtig ist, dass die Score-Werte des CHADS2 oder CHA2DS2-VASc nicht einfach mit denen des HAS-BLED verrechnet werden können: Bei dem mit dem Score erfassten Blutungsrisiko betrifft nur jede fünfte bis dritte die besonders relevanten intrakraniellen Blutungen.13 Zudem besteht eine hohe Korrelation zwischen Blutungsrisiko und Insultrisiko, so dass Patienten mit hoher Gefahr für eine Blutung unter Antikoagulation in der Regel auch am meisten von dieser profitieren.17 Nach Kalkulationen im Rahmen einer schwedischen Kohortenstudie, in der intrakranielle Blutungen besonders gewichtet werden, überwiegt der Nutzen einer oralen Antikoagulation den Schaden nur dann, wenn das Insultrisiko über 1% pro Jahr liegt.30 Ob allerdings dann immer bereits eine orale Antikoagulation indiziert ist, kann bezweifelt werden. Letztlich muss die Entscheidung zusammen mit dem Patienten getroffen werden. In diesem Rahmen sind Scores für Blutungs- und Insultrisiko sicher hilfreich.
| ** | HAS-BLED-Score (9 Punkte maximal)30 = Hypertonus, abnorme Nierenfunktion, abnorme Leberfunktion, Schlaganfall, Blutung, labile INR-Werte, Alter ≥ 65 (elderly), Drogen, die das Blutungsrisiko erhöhen: 1. Alkohol, 2. Arzneimittel wie Aggregationshemmer oder NSAR = je 1 Punkt |
Ein Nutzen von Azetylsalizylsäure (ASS; ASPIRIN, Generika) bei Patienten mit nichtvalvulärem Vorhofflimmern ist unsicher und allenfalls gering, wenn bisher keine transitorischen ischämischen Attacken (TIA) oder Insulte bekannt sind. Nach TIA oder Insult ist ein - allerdings begrenzter - Nutzen belegt. Ob ASS von Nutzen ist, wenn ausschließlich andere in Scores erfasste Risiken vorliegen, ist durch randomisierte Studien nicht belegt.
Cumarin-Antikoagulanzien verhindern bei Patienten mit nichtvalvulärem Vorhofflimmern mit oder ohne TIA oder Insult in der Anamnese Insulte oder systemische Embolien sicherer und deutlicher als ASS.
Unabhängig von TIA oder Insult in der Anamnese erhöht ASS die Rate schwerer und intrakranieller Blutungen, jedoch geringer als Cumarine. Hinweise, dass ASS gleich häufig zu schweren Blutungen führen soll wie Cumarine, entstammen überwiegend Beobachtungsstudien und sind nur bedingt aussagekräftig.
Weder in den Studien zur Prüfung von ASS noch in denen zu Cumarinen oder neuen oralen Antikoagulanzien wurden die Patienten mit Hilfe von Score-Werten für das Insultrisiko ausgewählt. In Leitlinien verwendete Algorithmen zur antithrombotischen Therapie an Hand von Risikoscores basieren somit überwiegend auf Analogieschlüssen.
Der CHADS2- und der CHA2DS2-VASc-Score beruhen auf epidemiologischen Daten. Über den Gesamtbereich ist ihr Vorhersagewert für das Insultrisiko vergleichbar. Im Bereich CHADS2 = 0-1 diskriminiert der CHA2DS2-VASc das Insultrisiko besser.
Einführung und Propagierung des CHA2DS2-VASc-Score haben zum Ziel, die Indikation für orale Antikoagulanzien bei Vorhofflimmern auszuweiten. Sie gehen auffällig parallel mit entsprechenden Empfehlungen für Dabigatran (PRADAXA) und Rivaroxaban (XARELTO) sowie zunehmendem Abraten von ASS.
Umsetzung der aktualisierten europäischen Leitlinie, ab Werten von 1 im CHA2DS2-VASc - entsprechend einem Insultrisiko von 1% pro Jahr - zu antikoagulieren, beträfe mehr als 90% aller Patienten mit nichtvalvulärem Vorhofflimmern. Bisher gibt es keine Belege, dass eine solche Strategie mehr nutzt als schadet.
Auch im Wissen um die Unsicherheiten bei Verwendung von Scores für therapeutische Entscheidungsfindungen raten wir wie nordamerikanische Leitlinien weiter ab einem CHADS2-Score von 2 zur Antikoagulation. Bei Werten von 0-1 sollte die Indikation an den konkreten Risiken der Patienten für Insulte und Blutungen ausgerichtet werden.
Für ASS sehen auch wir bei nichtvalvulärem Vorhofflimmern nur noch einen begrenzten Stellenwert.
| (M = Metaanalyse) | |
| M 1 | HART, R.G. et al.: Ann. Intern. Med. 2007; 146: 857- |
| M 2 | YOU, J.J. et al.: Chest 2012; 141 (Suppl): e531S-75S |
| M 3 | OWEN, A.: Int. J. Cardiol. 2010; 142: 218-23 |
| M 4 | AGUILAR, M., HART, R.: Antiplatelet therapy for preventing stroke in patients with non-valvular atrial fibrillation and no previous history of stroke and transient ischemic attacks. The Cochrane Database of Systematic Reviews, Stand Juni 2005; Zugriff Sept. 2012 |
| M 5 | AGUILAR, M.I. et al.: Oral anticoagulants versus antiplatelet therapy for preventing stroke in patients with non-valvular atrial fibrillation and no history of stroke or transient ischemic attacks. The Cochrane Database of Systematic Reviews, Stand Sept. 2006; Zugriff Sept. 2012 |
| M 6 | van WALRAVEN, C. et al.: JAMA 2002; 288: 2441-8 |
| 7 | GAGE, B.F. et al.: JAMA 2001; 285: 2864-70 |
| 8 | LIP, G.Y.H. et al.: Chest 2010; 137: 263-72 |
| 9 | CAMM, A.J. et al.: Eur. Heart J. 2012; online publ. am 24. Aug. 2012 |
| 10 | CAMM, A.J. et al.: Eur. Heart J. 2010; 31: 2369-429 |
| 11 | SKANES, A.C. et al.: Can. J. Cardiol. 2012; 28: 125-36 |
| 12 | FUSTER, V. et al.: J. Am. Coll. Cardiol. 2011; 57: e101-98 |
| 13 | FRIBERG, L. et al.: Eur. Heart J. 2012; 33: 1500-10 |
| 14 | OGILVIE, J.M. et al.: Thromb. Haemost. 2011; 106: 34-44 |
| 15 | KARTHIKEYAN, G., EIKELBOOM, J.W.: Thromb. Haemost. 2010; 104: 45-8 |
| M 16 | KEOGH, C. et al.: Thromb. Haemost. 2011; 106: 528-38 |
| 17 | PICCINI, J.P., SINGER, D.E.: Eur. Heart J. 2012; 33: 1431-3 |
| 18 | OLESEN, J.B. et al.: Thromb. Haemost. 2012; 107: 1172-9 |
| 19 | van STAA, T.P. et al.: J. Thromb. Haemost. 2010; 9: 39-48 |
| 20 | OLESEN, J.B. et al.: Brit. Med. J. 2011; 342: d124 (9 Seiten) |
| 21 | OLESEN, J.B. et al.: Chest 2012; 141: 147-53 |
| 22 | TSADOK, M.A. et al.: JAMA 2012; 307: 1952-8 |
| 23 | FRIBERG, L. et al.: Brit. Med. J. 2012; 344: e3522 (10 Seiten) |
| 24 | OLESEN, J.B. et al.: N. Engl. J. Med. 2012; 367: 625-35 |
| 25 | TRAPPE, H.J.: Dtsch. Ärztebl. 2012; 109: 1-7 |
| 26 | FURIE, K.L. et al.: Stroke 2012; online publ. am 2. Aug. 2012 |
| 27 | MASON, P.K. et al.: Am. J. Med. 2012; 125: 603.e1-6 |
| 28 | PISTERS, R. et al.: Chest 2010; 138: 1093-110 |
| 29 | OLESEN, J.B. et al.: Thromb. Haemost. 2011; 106: 739-49 |
| 30 | FRIBERG, L. et al.: Circulation 2012; 125: 2298-307 |
© 2012 arznei-telegramm, publiziert am 14. September 2012
Autor: angegebene Leser bzw. Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
