POSTMENOPAUSALE HORMONTHERAPIE | ||||||
Spätestens mit der Publikation der großen US-amerikanischen randomisierten plazebokontrollierten WHI*-Studie1 2002 wurde die bis
dahin vorherrschende Lehrmeinung, nach der die postmenopausale Hormontherapie Frauen vor Herzinfarkt schützt, gründlich erschüttert. Diese
These stützte sich ausschließlich auf Beobachtungsstudien und auf Studien mit Surrogatendpunkten wie Blutfettwerte (a-t 1995; Nr. 4: 37-44 und 2002; 33: 81-3).
DIE FALSCHEN MITTEL, DIE FALSCHEN FRAUEN? Die Ergebnisse der WHI-Studie sind in der gynäkologischen Fachwelt auf großen
Widerstand gestoßen. Für die hiesige Praxis seien sie nicht relevant, weil die falschen Mittel, die hier nur eine untergeordnete Rolle spielten, und die
falschen Frauen, die hier wegen ihres zu hohen Alters üblicherweise gar nicht behandelt würden, untersucht worden seien, so die beiden wichtigsten,
auch andernorts immer wieder vorgetragenen Einwände (a-t 2002; 33: 81-3).16,38 Randomisierte
kontrollierte Endpunktstudien, die die Sicherheit der hierzulande bevorzugt verwendeten Hormonpräparate und -Dosierungen belegen, gibt es jedoch nicht.
Solange solche Daten fehlen, wird man die für konjugierte Östrogene und Medroxyprogesteronazetat nachgewiesenen Schädigungspotenziale auch
bei anderen Östrogen-Gestagen-Kombinationen annehmen müssen, zumal viele der Risiken auch in Beobachtungsstudien beschrieben werden, in denen
ein breiteres Spektrum von Hormonpräparaten untersucht wird. Die Arzneimittelbehörden haben denn auch entsprechende Warnungen in die
Fachinformationen der Hormonpräparate aufgenommen.17,18
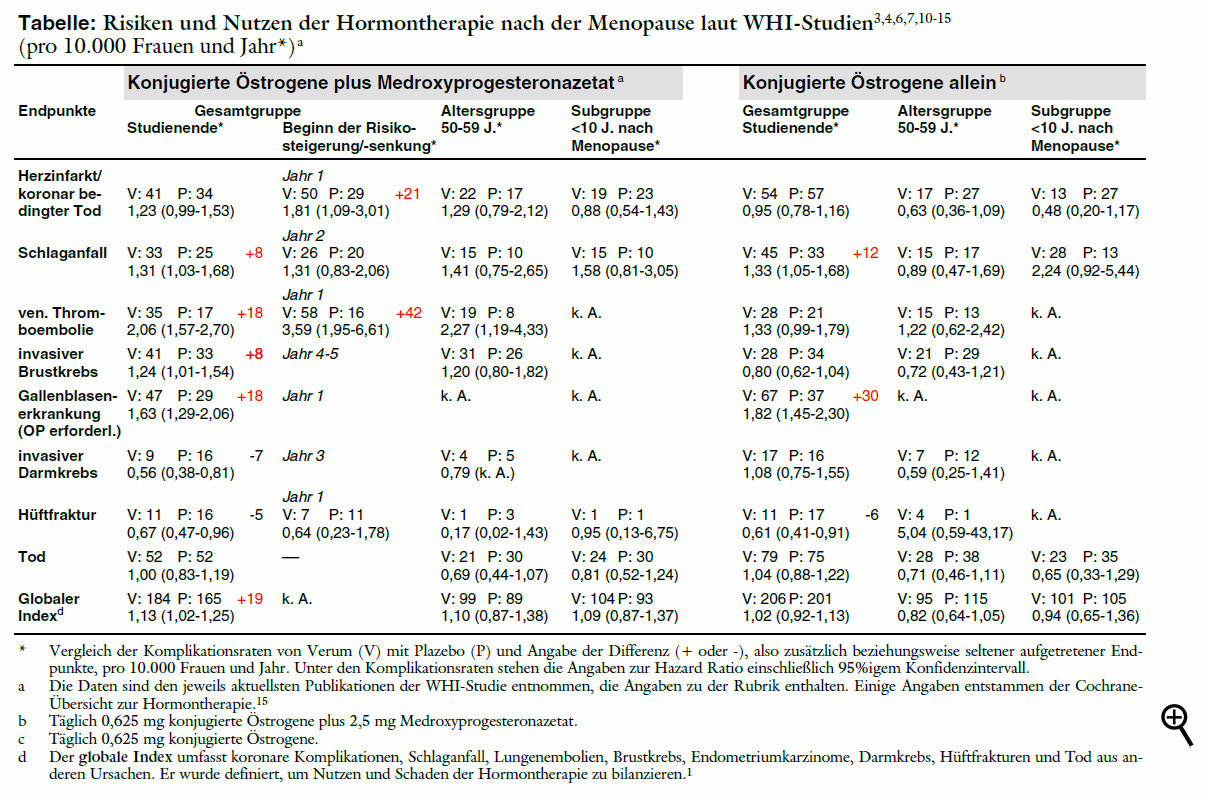
Das wesentliche methodische Element einer randomisierten kontrollierten Studie ist die Zuteilung zu Interventions- oder Kontrollgruppe nach dem Zufallsprinzip. Dadurch sollen systematische Unterschiede z.B. im Risikoprofil zwischen den Vergleichsgruppen vermieden werden, die nicht auszuschließen sind, wenn man Gruppen nur beobachtet, die sich selbst für oder gegen eine Anwendung entschieden haben. Der Randomisierungseffekt bleibt auch erhalten, wenn eine Verblindung nicht oder nur ungenügend möglich ist, wie zum Beispiel bei der Prüfung von Betablockern. Zwar können die Ergebnisse in offenen randomisierten Studien durch einen so genannten Detection-Bias verzerrt sein, wenn zum Beispiel durch häufigeres Screening in einer Gruppe hier mehr Erkrankungen entdeckt werden. Die Unterstellung eines Detection-Bias als Ursache für die höhere Herzinfarktrate unter kombinierter Hormontherapie in der WHI-Studie bleibt jedoch Spekulation. Wenn das Wissen um die Zuteilung zu Verum die Erwartungshaltung der Studienteilnehmerinnen verändert hätte, dann wäre bei der in den 1990er Jahren vorherrschenden Überzeugung, dass Hormone vor Herzinfarkt schützen, eher mit der gegenteiligen Reaktion, nämlich einer Beruhigung, zu rechnen gewesen. Für den unterstellten Einfluss der Ergebnisse der HER-Studie31 bleiben die Autoren die Belege schuldig. Auf die Häufigkeit der Hormonverordnungen in den USA hatte die Publikation 1998 jedenfalls keinen unmittelbaren Effekt.21 Zum Zeitpunkt der Warnung durch die WHI-Autoren 2000 und 2001 waren alle Frauen bereits länger als ein Jahr in der Studie. Im ersten Studienjahr ist der Risikoanstieg jedoch am höchsten. Nach Auskunft des Erstautors der WHI-Studie ist der unter Verum beobachtete Anstieg des Herzinfarktrisiko bei den Frauen, deren Gynäkologen vor allem wegen vaginaler Blutungen entblindet wurden, geringer als bei den Frauen, deren Gynäkologen nicht entblindet wurden.34 Auch zwei aktuelle nachträgliche Auswertungen der WHI-Studien12,35 können aus methodischen Gründen eine günstigere Nutzen- Risiko-Bilanz der Hormontherapie bei jüngeren Frauen nicht belegen. Bei der einen handelt es sich um eine gepoolte Analyse der beiden WHI-Arme mit Östrogen plus Gestagen und Östrogen allein. In der Subgruppe der 50- bis 59-Jährigen ergibt sich in dieser Auswertung im Unterschied zu älteren Frauen kein erhöhtes Herzinfarktrisiko unter Hormonen, in der Subgruppe der Frauen, deren Menopause weniger als zehn Jahre zurückliegt, ein Trend zur Risikoreduktion. Signifikant sind die Unterschiede zwischen jüngeren und älteren Frauen jedoch auch in dieser Analyse nicht. Die Auswertung der gepoolten Daten in den Subgruppen zur Zeitspanne seit Menopause ist zudem nachträglich geplant und wird wegen fehlender Daten unter Ausschluss von 11% der Frauen durchgeführt.12 Zweifelhaft erscheint uns jedoch vor allem, dass sich aus den gepoolten Daten der beiden Studienarme überhaupt sinnvolle Aussagen ableiten lassen: Beim derzeitigen Kenntnisstand muss das zusätzliche Gestagen als Ursache für die ungünstigeren Ergebnisse unter der kombinierten Therapie mit verantwortlich gemacht werden. Durch Poolen mit den Ergebnissen der offensichtlich weniger riskanten Monotherapie, die aber nur für eine Minderheit der Frauen infrage kommt, werden die Risikosignale, die sich aus der WHI-Studie für die kombinierte Therapie ergeben, verwässert. Bei der zweiten Arbeit handelt es sich um eine nachträglich geplante Zusatzstudie des WHI-Arms zur Monotherapie, in der Frauen, die zu Studienbeginn 50 bis 59 Jahre alt waren, mehr als ein Jahr nach Abschluss computertomographisch auf Verkalkung der Koronarien untersucht werden, die bei den ehemaligen Verumanwenderinnen weniger weit fortgeschritten sein soll als in der ehemaligen Plazebogruppe.35 Abgesehen davon, dass ein Surrogatendpunkt geprüft wird, wird die Aussagekraft dieser Studie vor allem auch dadurch eingeschränkt, dass Befunde vor Behandlung fehlen und weniger als 50% der ursprünglich randomisierten Frauen daran teilnehmen. Durch die beiden neuen WHI-Arbeiten sehen sich die Verfechter der so genannten "Timing-Hypothese" bestätigt: Danach beugt die Hormontherapie einer Atherosklerose vor, jedoch nur dann, wenn sie frühzeitig nach der Menopause begonnen wird, bevor sich atherosklerotische Gefäßschäden ausgebildet haben. Diese These wurde aufgrund von experimentellen Daten und Befunden aus Tierversuchen entwickelt.36 Tierversuche, Surrogatparameter und Subgruppenanalysen ohne statistische Aussagekraft reichen jedoch nicht aus, um über die Timing-Hypothese zuverlässige Aussagen zu machen. Wir sehen daher derzeit keine hinreichenden Gründe zur Neubewertung der Hormontherapie bei jungen Frauen. Frauen, die wegen Wechseljahresbeschwerden eine Hormontherapie wünschen, müssen wissen, dass die beste verfügbare Evidenz derzeit auch bei kurzzeitiger Anwendung von Östrogenen plus Gestagenen für ein erhöhtes Thromboembolie- und Herzinfarktrisiko spricht und dass bei mehrjähriger Anwendung auch das Schlaganfallrisiko sowie das Risiko von Gallenblasenerkrankungen zunimmt. Der Anstieg des Brustkrebsrisikos wird in der WHI-Studie zwar auch erst nach mehrjähriger Hormoneinnahme sichtbar (siehe Tabelle, Seite 66), dabei ist jedoch zu berücksichtigen, dass die erhöhte Strahlendichte des Brustgewebes unter Östrogen-Gestagen-Therapie Brustkrebsdiagnosen erschwert und verzögert hat. Ob es ein Zeitfenster gibt, in dem ein erhöhtes Brustkrebsrisiko sicher nicht besteht, bleibt daher offen. Auch unter der offenbar etwas weniger schädlichen Östrogen-Monotherapie bei Frauen nach Hysterektomie muss mit erhöhtem Risiko von Schlaganfällen und Gallenblasenoperationen, wahrscheinlich auch von Thromboembolien gerechnet werden. In den Fachinformationen wird zudem auch vor erhöhtem Brustkrebsrisiko unter Östrogenen allein gewarnt. Die Frauen müssen zudem wissen, dass Wechseljahresbeschwerden nach Absetzen einer Hormontherapie wiederkehren können. Nach Daten aus der WHI-Studie ist dies bei mehr als der Hälfte der Frauen der Fall. Dies spricht dafür, dass die Beschwerden nicht überbrückt, sondern lediglich verschoben werden (a-t 2005; 36: 69-71).37 |
| (R= randomisierte Studie, M= Metaanalyse) | |
R |
1 |
Writing Group for the Women's Health Initiative Investigators: JAMA 2002; 288: 321- 33 |
R |
2 |
HULLEY, S. et al.: JAMA 1998; 280: 605-13 |
R |
3 |
MANSON, J.E. et al.: N. Engl. J. Med. 2003; 349: 523-34 |
R |
4 |
CUSHMAN, M. et al.: JAMA 2004; 292: 1573-80 |
R |
5 |
WASSERTHEIL-SMOLLER, S. et al.: JAMA 2003; 289: 2673-84 |
R |
6 |
CHLEBOWSKI, R.T. et al.: JAMA 2003; 289: 3243-53 |
R |
7 |
CIRILLO, D.J. et al.: JAMA 2005; 293: 330-9 |
R |
8 |
HENDRIX, S.L. et al.: JAMA 2005; 293: 935-48 |
R |
9 |
SHUMAKER, S.A. et al.: JAMA 2003; 289: 2651-62 |
R |
10 |
CAULEY, J.A. et al.: JAMA 2003; 290: 1729-38 |
R |
11 |
CHLEBOWSKI, R.T. et al.: N. Engl. J. Med. 2004; 350: 991-1004 |
M |
12 |
ROSSOUW, J.E. et al.: JAMA 2007; 297: 1465-77 |
R |
13 |
The Women's Health Initiative Steering Committee: JAMA 2004; 291: 1701-12 |
R |
14 |
STEFANICK, M.L. et al.: JAMA 2006; 295: 1647-57 |
M |
15 |
FARQUAR, C.M. et al.: Long term hormone therapy for perimenopausal and postmenopausal women. The Cochrane Database of Systematic Reviews 2007, Issue 2; Stand Mai 2005 |
|
16 |
BARRETT-CONNOR, E.: J. Clin. Endocrinol. Metab. 2003; 88: 4031-42 |
|
17 |
Bundesinstitut für Arzneimittel und Medizinprodukte: Pressemitteilung vom 18. Aug. 2003: http://www.bfarm.de/cln_042/nn_421158/DE/Presse/ mitteil2003/pm18-2003.html__nnn=true |
|
18 |
FDA: "Estrogen and Estrogen with Progestin Therapies for Postmenopausal Women", Stand Febr. 2007: http://www.fda.gov/cder/drug/infopage/estrogens_progestins/ |
R |
19 |
HSIA, J. et al.: Arch. Intern. Med. 2006; 166: 357-65 |
|
20 |
Deutsche Gesellschaft für Gynäkologie und Geburtshilfe, Berufsverband der Frauenärzte: Konsensusempfehlungen zur Hormontherapie (HT) im Klimakterium und in der Postmenopause, Stand Mai 2004; http://www.dggg.de/leitlinien-2006/pdf-2006/3-endo-fpm/3-1-2-1- hrt-konsensus.pdf |
|
21 |
HERSH, A.L. et al.: JAMA 2004; 291: 47-53 |
|
22 |
Robert Koch-Institut: Pressemitteilung vom 28. Juni 2007 |
|
23 |
RAVDIN, P.M. et al.: N. Engl. J. Med. 2007; 356: 1670-4 |
|
24 |
KATALINIC, A., RAWAL, R.: Breast Cancer Res. Treat. 2007, online publ. Juni 2007 |
|
25 |
KATALINIC, A., RAWAL, R.: Kongressbeitrag Lübeck, Saarbrücken, Juni 2007 |
|
26 |
Deutsche Gesellschaft für Gynäkologie und Geburtshilfe und andere Fachgesellschaften: Anwendungsempfehlungen zur Hormonersatztherapie im Klimakterium und in der Postmenopause, Stand Sept. 2006; http://www.dggg. de/leitlinien2006/pdf-2006/3-endo-fpm/3 -1-2-1a-hrt-empfehlung2006.pdf |
|
27 |
EMONS, G.: Vortrag Symposium Hormontherapie bei (post-) menopausalen Frauen in Deutschland 2007, Berlin, 27. Juni 2007 |
|
28 |
Stuttgarter Nachrichten vom 22. Nov. 2006 |
|
29 |
MUECK, A.O.: Schreiben vom 27. Nov. 2006 |
|
30 |
SHAPIRO, S.: Climacteric 2003; 6: 302-10 |
|
31 |
GARBE, E., SUISSA, S.: Hum. Reprod. 2004; 19: 8-13 |
|
32 |
HEINEMANN, L.A.J.: Frauenarzt 2004; 45: 217-22 |
M |
33 |
SALPETER, S.R. et al.: J. Gen. Intern. Med. 2006; 21: 363-6 |
|
34 |
ROSSOUW, J.E.: Schreiben vom 5. Juli 2007 |
|
35 |
MANSON, J.E. et al.: N. Engl. J. Med. 2007; 356: 2591-602 |
|
36 |
MENDELSOHN, M.E., KARAS, R.H.: N. Engl. J. Med. 2007; 356: 2639-41 |
|
37 |
OCKENE, J.K. et al.: JAMA 2005; 294: 183-93 |
|
38 |
HEMMINKI, E.: Health Policy 2004; 69: 283-91 |
| © 2007 arznei-telegramm |
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
